Генотип шизофрении ограничили 413 генами
Международная группа ученых обнаружила 413 генов, экспрессия которых в головном мозге связана с шизофренией. Для этого они создали статистическую модель, которая связывает характерную для заболевания экспрессию генов в головном мозге с генетическими вариантами по всему геному. Вовлеченные в заболевание гены затем обнаружили, проанализировав геном более сотни тысяч человек, у 40 тысяч из которых диагностирована шизофрения. Статья опубликована в журнале Nature Genetics.
Шизофрения — одно из самых плохо изученных психических заболеваний. Сложности заключаются как в его диагностике (до сих пор не выявлено единой симптоматики заболевания), так и в изучении и лечении: исследования шизофрении сильно осложнены тем, что вывести модельные организмы с достоверными симптомами заболевания практически невозможно. Применяемые сейчас антипсихотики позволяют только купировать некоторые симптомы.
Известно, что шизофрения — заболевание наследуемое, но до сих пор генетические исследования этого вопроса не давали точных результатов (подробнее об этом вы можете прочитать в нашем материале «Безумие в наследство»), хотя метод полногеномного поиска ассоциаций несколько раз указывал на наличие некоторых генов-кандидатов (об этом вы можете прочитать во второй части материала, «Безумие в наследство — 2»). Тем не менее, сам метод может указать только на связь определенного генотипа (а точнее — однонуклеотидных полиморфизмов) с риском развития заболевания и проявления определенных симптомов, но не могут дать информации об экспрессии определенных генов в тканях.
Тем не менее, сам метод может указать только на связь определенного генотипа (а точнее — однонуклеотидных полиморфизмов) с риском развития заболевания и проявления определенных симптомов, но не могут дать информации об экспрессии определенных генов в тканях.
Ученые под руководством Лоры Хакинс (Laura Huckins) из Медицинской школы Икан на горе Синай (Нью-Йорк) решили расширить и систематизировать имеющиеся данные о генетических маркерах шизофрении. Они использовали статистический метод транскриптомной импутации (transcriptomic imputation), который помогает обнаружить взаимосвязь между результатами полногеномных исследований и исследований транскриптома, которые связывают экспрессию генов в тканях с определенными признаками, характерными для организма. Другими словами, такой метод позволяет не только выявить генетические вариации, характерные для определенного состояния, но и выделить среди них те, экспрессия которых в тканях в действительности связана с проявлением симптомов заболевания.
Для этого ученые воспользовались посмертными данными, собранными в рамках проекта CommonMind Consortium: оттуда они взяли данные о генотипе и экспрессии генов в доросатеральной части префронтальной коры головного мозга 538 человек (254 из них болели шизофренией). Они создали статистическую модель, которая предсказывает экспрессию определенного гена в тканях головного мозга на основе наличия определенных однонуклеотидных полиморфизмов (то есть как раз на основе данных полногеномного анализа). Всего с помощью такого анализа ученым удалось выделить около 20 тысяч уникальных генов, варианты которых могут быть связаны с экспрессией генов в префронтальной коре — в основном, через влияние на другие участки мозга.
Для того, чтобы сузить характерный для шизофрении генотип, ученые проанализировали геном 40299 человек с диагностированной шизофренией и 65264 здоровых человек в качестве контрольной группы. На основании этого ученым удалось выделить 413 генетических вариантов с экспрессией в 13 участках мозга, включая как дорсолатеральную часть префронтальной коры, так и, к примеру, мозжечок, гиппокам, гипоталамус, базальную ганглию и другие.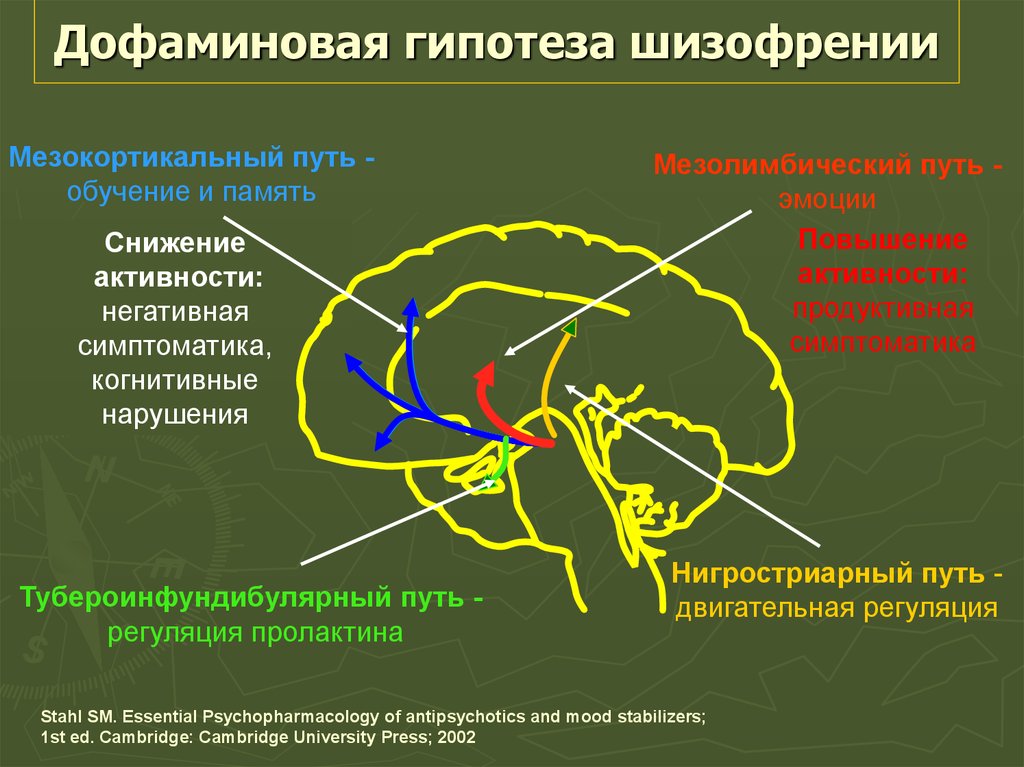 Воспользовавшись данными об экспрессии генов в головном мозге в разные периоды развития организма человека (от раннего утробного до взрослого возраста), исследователи также оценили и то, как экспрессия в изученных участках проявляется в течение жизни человека. Так, в самом начале формирования мозга в утробе матери наиболее значимая экспрессия, характерная для шизофрении, наблюдается в первичной соматосенсорной и моторной коре, а также в дорсолатеральной и вентролатеральной частях префронтальной коры.
Воспользовавшись данными об экспрессии генов в головном мозге в разные периоды развития организма человека (от раннего утробного до взрослого возраста), исследователи также оценили и то, как экспрессия в изученных участках проявляется в течение жизни человека. Так, в самом начале формирования мозга в утробе матери наиболее значимая экспрессия, характерная для шизофрении, наблюдается в первичной соматосенсорной и моторной коре, а также в дорсолатеральной и вентролатеральной частях префронтальной коры.
Крупные генетические исследования очень важны для изучения таких наследуемых заболеваний, как шизофрения. Метод, который применили ученые в новой работе, позволяет существенно сократить количество генов, которые в действительности влияют на риск развития заболевания через экспрессию в тканях, тем самым делая генетический анализ более точным.
Зимой прошлого года другое крупное исследование экспрессии генов в головном мозге при наличии психических заболеваний сблизили шизофрению и биполярное расстройство. Об этом вы можете прочитать в нашей заметке.
Об этом вы можете прочитать в нашей заметке.
Елизавета Ивтушок
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Шизофрению вызывают два мутировавших гена — РБК
adv.rbc.ru
adv.rbc.ru
adv.rbc.ru
Скрыть баннеры
Ваше местоположение ?
ДаВыбрать другое
Рубрики
Курс евро на 3 декабря
EUR ЦБ: 64,99
(+1,16)
Инвестиции, 02 дек, 16:04
Курс доллара на 3 декабря
USD ЦБ: 61,77
(+0,63)
Инвестиции, 02 дек, 16:04
Bloomberg узнал о планах ФРГ купить сверхзвуковые истребители за €10 млрд Политика, 04:04
Во Всемирном банке предупредили о росте числа бедных на Украине до 8 млн Общество, 03:44
В Госдуме предложили разрешить директорам школ досрочный выход на пенсию Общество, 03:38
adv. rbc.ru
rbc.ru
adv.rbc.ru
Центробанки ФРГ и Франции пообещали снизить инфляцию до 2% за три года Экономика, 03:19
Клишас допустил ограничения для уехавших после начала мобилизации россиян Политика, 02:32
Британский министр призвал врачей не бастовать для «сигнала Путину» Политика, 02:26
Подоляк сообщил о начале национализации бывшего «Альфа-Банк Украина» Бизнес, 01:46
Объясняем, что значат новости
Вечерняя рассылка РБК
Подписаться
Интеллигентность — это про чувство вкуса. Как ее оценить РБК и ГАЛС, 01:41
Вильфанд назвал срок начала потепления в европейской части России Общество, 01:39
ТАСС узнал о семи пропавших после обрушения части дома в Нижневартовске Общество, 01:14
Аналитики назвали улицы Москвы с самым дорогим жильем Недвижимость, 01:00
Драка с участием Лепса произошла у бара в Санкт-Петербурге Общество, 00:50
Безвизовый рай для сноубордистов: как выбрать зимний курорт в Корее РБК и НОТК, 00:45
Республиканцы начали расследование «секретной сделки» с Эр-Риядом о нефти Политика, 00:41
adv. rbc.ru
rbc.ru
adv.rbc.ru
adv.rbc.ru
Ученые так и не могут сойтись во мнении, что же вызывает шизофрению – ретровирус или мутация генов? А может быть, еще какой-то не известный науке фактор? Ирландские и исландские ученые убеждены, что во всем виноваты генетические мутации, и они уже практически обнаружили гены, виновные в возникновении этой болезни.
Исследователи психических болезней человека полагают, что они как никогда ранее близки к разгадке причин возникновения шизофрении. Ученые из университета Ричмонда и их ирландские коллеги проанализировали генные коды 270 ирландских семей, в которых имеются больные шизофренией. Этот проект начался в 1983 году и представлял собой изучение историй болезней в каждой психиатрической клинике Ирландии, включая Северную Ирландию, кроме Белфаста. По утверждению ученых, они обнаружили «ключик», который указывает на определенный ген – дисбиндин – который, по их мнению, отвечает за передачу, возникновение и развитие шизофрении. Этот ген расположен на шестой паре хромосом из имеющихся у человека двадцати трех пар. А в это время ученые из исландской компании Decode Genetics в своем независимом исследовании обнаружили другой ген, неурегулин-1, расположенный на восьмой паре хромосом. Они утверждают, что мутации этого гена напрямую связаны с шизофренией. Такие данные были получены в результате анализа исландских семей, имеющих в истории болезни шизофрению — 15% больных этим недугом имеют мутированный неурегулин-1. Профессор Кари Стефанссон, генеральный директор компании Decode Genetics в Рейкьявике, убежден, что шизофрения является плодом мутации двух генов, дисбиндина и неурегулина-1, которые имеют какую-то, пока что не установленную, связь. По мнению профессора, эти гены участвуют в регуляции синапсов, при этом один нейрон сплетается с другим. В результате происходит мутация, которая нарушает нормальное функционирование нейронов мозга, и, как следствие, у человека с подобной мутацией генов, возникает расстройство психики.
Этот ген расположен на шестой паре хромосом из имеющихся у человека двадцати трех пар. А в это время ученые из исландской компании Decode Genetics в своем независимом исследовании обнаружили другой ген, неурегулин-1, расположенный на восьмой паре хромосом. Они утверждают, что мутации этого гена напрямую связаны с шизофренией. Такие данные были получены в результате анализа исландских семей, имеющих в истории болезни шизофрению — 15% больных этим недугом имеют мутированный неурегулин-1. Профессор Кари Стефанссон, генеральный директор компании Decode Genetics в Рейкьявике, убежден, что шизофрения является плодом мутации двух генов, дисбиндина и неурегулина-1, которые имеют какую-то, пока что не установленную, связь. По мнению профессора, эти гены участвуют в регуляции синапсов, при этом один нейрон сплетается с другим. В результате происходит мутация, которая нарушает нормальное функционирование нейронов мозга, и, как следствие, у человека с подобной мутацией генов, возникает расстройство психики.
Дальнейшие исследования в этой области, возможно, позволят найти лекарство от шизофрении. Это уже будут не лекарственные препараты, а применение генной инженерии – то есть не снятие симптомов, а ликвидация причины заболевания.
Ananova
специфических генов, ответственных за шизофрению, идентифицированы впервые | Новости ЛЧ
Знаменательное исследование, проведенное с участием ученых из Калифорнийского университета Лондона, впервые выявило десять генов с чрезвычайно редкими мутациями, разрушающими белок, которые значительно повышают риск развития шизофрении у человека.
В связанной статье, опубликованной в Nature , исследователи также выявили беспрецедентное количество генетических связей с шизофренией в человеческом геноме — схеме ДНК тела.
Результаты являются результатом совместной работы сотен исследователей из 45 стран, которые проанализировали ДНК 76 755 человек с шизофренией и 243 649 человек без нее, чтобы лучше понять гены и биологические процессы, лежащие в основе этого состояния.
В то время как предыдущие исследования показали связь между шизофренией и многими областями ДНК, это первое исследование, в котором определены конкретные гены.
Исследователи говорят, что исследования являются прорывом в нашем понимании основ шизофрении. и предоставить самые убедительные доказательства генетической причины.
Профессор Эндрю Маккуиллин, соавтор* статей и глава Лаборатории молекулярной психиатрии UCL (Отделение психиатрии UCL), сказал: «Теперь мы смогли обнаружить определенные гены, что является необходимым шагом на сложном пути к пониманию Причины и механизмы любого расстройства.
«Хотя существует большое количество генетических вариантов, связанных с шизофренией, исследования показали, что они сконцентрированы в генах, экспрессированных в нейронах. Как редкие мутации высокого риска, так и распространенные генетические варианты низкого риска непротиворечивы и указывают нам на такие гены, как GRIN2A, также важные при эпилепсии и нарушениях развития нервной системы».
Шизофрения — это психическое расстройство, которым страдает примерно один из 300 человек во всем мире. По данным Всемирной организации здравоохранения, двое из каждых трех человек с шизофренией и другими психозами не получают специализированной психиатрической помощи.
Два исследования были проведены Консорциумом SCHEMA и Консорциумом психиатрической геномики, которые являются крупнейшим международным сотрудничеством в области психического здоровья.
В докладе Консорциума SCHEMA впервые были выявлены чрезвычайно редкие мутации, разрушающие белок, в 10 генах, которые сильно повышают риск развития шизофрении у человека — в одном случае более чем в 30 раз. В этой статье использовалось крупномасштабное секвенирование экзома: передовая технология, позволяющая идентифицировать специфические гены, вовлеченные в шизофрению.
Консорциум психиатрической геномики (PGC) обнаружил гораздо большее количество генетических связей с шизофренией, чем когда-либо прежде, в 287 различных областях генома. Они показали, что генетический риск шизофрении наблюдается в генах, сконцентрированных в нейронах, но не в какой-либо другой ткани или типе клеток, предполагая, что биологическая роль этих клеток имеет решающее значение при шизофрении.
Они показали, что генетический риск шизофрении наблюдается в генах, сконцентрированных в нейронах, но не в какой-либо другой ткани или типе клеток, предполагая, что биологическая роль этих клеток имеет решающее значение при шизофрении.
Помимо того, что это крупнейшее на сегодняшний день исследование геномики психического здоровья, в него были включены люди афроамериканского, латиноамериканского и европейского происхождения, что сделало шаг к более разнообразным и инклюзивным исследованиям как с точки зрения участников, так и ученых. PGC включает в себя коллег из Восточной и Южной Азии и быстро расширяется по всему миру, чтобы гарантировать, что достижения в области геномики приносят пользу людям всех предков.
Профессор Эльвира Брамон, соавтор* статьи PGC и глава отдела исследований в области неврологии психического здоровья (отделение психиатрии UCL), сказала: «Хотя у нас есть эффективные лекарственные и психологические вмешательства для лечения шизофрении и биполярного расстройства, многие люди испытывают побочные эффекты или их симптомы улучшаются лишь частично, что влияет на их физическое здоровье, благополучие и даже продолжительность жизни. Понимание генетики — ключевой шаг к разработке новых лекарств и адаптации уже имеющихся методов лечения для удовлетворения потребностей каждого человека».0003
Понимание генетики — ключевой шаг к разработке новых лекарств и адаптации уже имеющихся методов лечения для удовлетворения потребностей каждого человека».0003
Доктор Ник Басс (отделение психиатрии UCL), соавтор* статьи, сказал: «Данные секвенирования экзома идентифицируют AKAP11 как ген риска биполярного расстройства и шизофрении. Мы находим все больше доказательств генетического совпадения и общей биологии между этими двумя и другими распространенными расстройствами, такими как депрессия. Это важно, чтобы выйти за рамки симптомов, улучшить диагностику и быстро получить доступ к лечению».
Консорциум SCHEMA и Консорциум психиатрической геномики финансируются Национальным институтом психического здоровья (NIMH) США.
Доктор Джошуа Гордон, директор NIMH, сказал: «Эти результаты, достигнутые благодаря беспрецедентному по своим масштабам глобальному сотрудничеству, знаменуют собой важный шаг вперед в нашем понимании происхождения шизофрении. Полученные данные позволят исследователям сосредоточиться на конкретных путях мозга в продолжающейся охоте за новыми методами лечения этого серьезного психического заболевания».
Калифорнийский университет Лондона и другие университеты Великобритании внесли большой вклад в эти исследования благодаря тысячам участников, лабораторным работам и аналитическим материалам. Работа в UCL финансируется Советом по медицинским исследованиям, Wellcome, Mental Health Research UK, Институтом психического здоровья UCL и Центром биомедицинских исследований NIHR в UCLH.
* Профессор Эндрю МакКуиллин и доктор Ник Басс были соавторами статей Nature и Nature Genetics . Профессор Эльвира Брамон была соавтором PGC 9.0047 Бумага Nature .
Links
- All three Nature research papers will be published online shortly
- Professor Andrew McQuillin’s academic profile
- Professor Elvira Bramon’s academic profile
- Dr Nick Bass’ academic profile
- UCL Division of Psychiatry
- SCHEMA Consortium
- Консорциум психиатрической геномики
Изображение
- «Пожилая женщина держит в мозгу символ пропавшей головоломки», кредит ipopba на iStock
Контакты для СМИ
Henry Killworth
Тел. : +44 (0) 7881 833274
: +44 (0) 7881 833274
E: h.killworth [at] ucl.ac.uk
Schizophrenia Genes and Loci Identified генетические исследования с участием многих сотен тысяч участников выявили сотни областей генома, которые могут содержать гены, связанные с шизофренией. Одно из исследований выявило несколько генов с редкими мутациями, которые, по-видимому, связаны с расстройством.
Международный консорциум SCHEMA (SCHizophrenia Exome Meta-Analysis) во главе с исследователями из Института Броуда Массачусетского технологического института и Гарварда выявил чрезвычайно редкие мутации, разрушающие белок, в 10 генах. которые сильно увеличивают риск развития шизофрении у человека — в одном случае более чем в 20 раз. Вторая опубликованная работа, полногеномное ассоциативное исследование (GWAS) в более крупной, но перекрывающейся группе из 320 400 человек, была проведена Консорциумом психиатрической геномики (PGC), в который входят те же исследователи Броуда, и доводит количество областей до 287. генома, связанного с риском шизофрении, включая локусы, содержащие гены, идентифицированные SCHEMA.
генома, связанного с риском шизофрении, включая локусы, содержащие гены, идентифицированные SCHEMA.
Два исследования появляются рядом друг с другом в Nature . Вместе они подчеркивают формирующийся взгляд на шизофрению как на нарушение связи в синапсе (соединение между нейронами) и иллюстрируют, как различные виды генетических вариаций, влияющих на одни и те же гены, могут влиять на риск различных психических расстройств и нарушений развития нервной системы.
«Психические расстройства очень долгое время были черным ящиком», — сказал Тарджиндер Сингх, доктор философии, научный сотрудник Центра психиатрических исследований Стэнли в Институте Броуда. «В отличие от сердечно-сосудистых заболеваний или рака, у нас было очень мало биологических ключей к механизмам заболевания. В результате у нас не было необходимых знаний для разработки столь необходимых новых методов лечения. Вместо этого мы повторяем антипсихотические препараты, случайно открытые более 70 лет назад».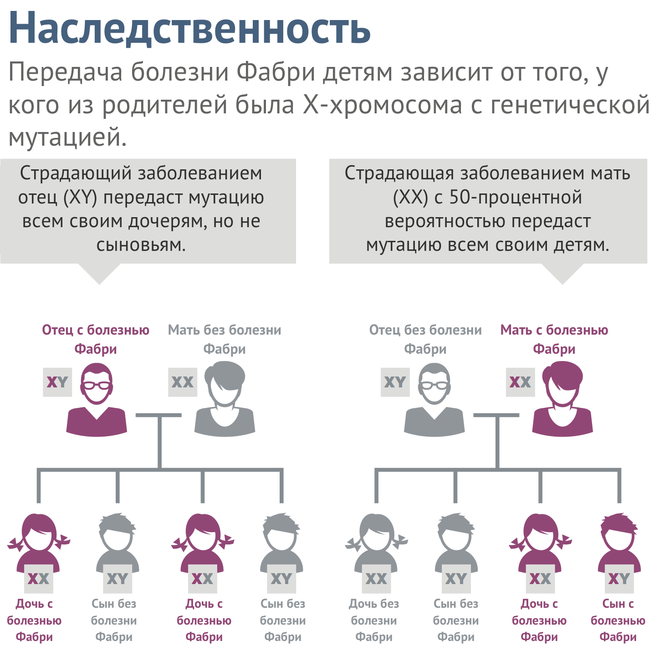 Сингх, который также работает в Отделе аналитической и трансляционной генетики (ATGU) Массачусетской больницы общего профиля, является первым и соавтором исследования SCHEMA под названием «Редкие варианты кодирования в генах придают значительный риск шизофрении». и соавтор исследования PGC под названием «Картирование геномных локусов указывает на участие генов и синаптической биологии в шизофрении».
Сингх, который также работает в Отделе аналитической и трансляционной генетики (ATGU) Массачусетской больницы общего профиля, является первым и соавтором исследования SCHEMA под названием «Редкие варианты кодирования в генах придают значительный риск шизофрении». и соавтор исследования PGC под названием «Картирование геномных локусов указывает на участие генов и синаптической биологии в шизофрении».
По словам Сингха, эти два исследования стали возможными, потому что необходимые части наконец были готовы. «Геномные технологии, инфраструктура секвенирования, вычислительные инструменты, необходимые для понимания данных, которые они производят, значительно продвинулись вперед за последние два десятилетия», — сказал он. «Самым важным моментом было глобальное обязательство со стороны членов PGC и SCHEMA по обмену образцами и данными между учреждениями и странами для достижения количества людей, необходимого для выявления этих редких мутаций».
Шизофрения — это серьезное психическое расстройство, которое начинается в позднем подростковом или раннем взрослом возрасте и в любой момент времени затрагивает примерно одного из 300 человек во всем мире, по данным Всемирной организации здравоохранения. Расстройство имеет наследуемость 60–80%, отметили авторы PGC, и «большая часть индивидуальных различий в риске является генетической и включает большое количество общих аллелей, вариантов с редким числом копий (CNV) и редких вариантов кодирования. ” И хотя есть потребность в новых терапевтических мишенях, этому процессу препятствует наше ограниченное понимание патофизиологии». Авторы SCHEMA согласились: «Отсутствие прогресса в терапевтических разработках отчасти является следствием ограниченного понимания молекулярной этиологии психического расстройства», — отмечают авторы SCHEMA.
Расстройство имеет наследуемость 60–80%, отметили авторы PGC, и «большая часть индивидуальных различий в риске является генетической и включает большое количество общих аллелей, вариантов с редким числом копий (CNV) и редких вариантов кодирования. ” И хотя есть потребность в новых терапевтических мишенях, этому процессу препятствует наше ограниченное понимание патофизиологии». Авторы SCHEMA согласились: «Отсутствие прогресса в терапевтических разработках отчасти является следствием ограниченного понимания молекулярной этиологии психического расстройства», — отмечают авторы SCHEMA.
Находки SCHEMA и PGC являются результатом десятилетней работы исследователей Центра Стэнли и почти четырех десятков других учреждений по всему миру. Оба проекта направлены на сбор и сравнение ДНК большого количества людей с шизофренией и без нее. Работая вместе, исследователи PGC создали набор данных, который теперь включает более 320 400 человек из коллекций по всему миру, включая людей европейского, финского, афроамериканского, латиноамериканского, восточноазиатского и ашкеназского еврейского происхождения. Когорта SCHEMA включает более 121 000 человек.
Когорта SCHEMA включает более 121 000 человек.
Две группы пошли взаимодополняющими путями в изучении генетики шизофрении. С 2009 года команда PGC проводит все более масштабные ассоциативные исследования по всему геному, каталогизируя однонуклеотидные полиморфизмы (SNP), которые способствуют риску шизофрении. В своем недавно опубликованном исследовании PGC заявила: «Мы выполнили самый крупный, насколько нам известно, GWAS шизофрении на сегодняшний день и при этом выявили значительное увеличение числа связанных локусов»
Консорциум SCHEMA (SCHizophrenia Exome Meta-Analysis), который объединился в 2017 году, занимается экзомом, почти 2% генома, который кодирует белки. В частности, консорциум SCHEMA искал варианты, которые либо отключали бы, либо заметно изменяли бы способность гена производить функционирующие белки.
Путем секвенирования полных экзомов от 24 248 человек с шизофренией и 97 322 без, команда SCHEMA выявила ультраредкие варианты в 10 генах, которые резко повышают риск развития шизофрении у человека. Эти варианты, называемые PTV для «вариантов укорочения белка», не позволяют клеткам производить полноразмерный функциональный белок гена. «В целом у любого человека есть примерно один процент шансов заболеть шизофренией в течение жизни», — сказал Бенджамин Нил, доктор философии, еще один соавтор исследования SCHEMA, сотрудник PGC, член института и директор отдела генетики в Стэнли Центра, соруководителя программы института в области медицинской и популяционной генетики и профессорско-преподавательского состава Mass General ATGU. «Но если у вас есть одна из этих мутаций, это становится шансом на 10, 20 или даже 50 процентов».
Эти варианты, называемые PTV для «вариантов укорочения белка», не позволяют клеткам производить полноразмерный функциональный белок гена. «В целом у любого человека есть примерно один процент шансов заболеть шизофренией в течение жизни», — сказал Бенджамин Нил, доктор философии, еще один соавтор исследования SCHEMA, сотрудник PGC, член института и директор отдела генетики в Стэнли Центра, соруководителя программы института в области медицинской и популяционной генетики и профессорско-преподавательского состава Mass General ATGU. «Но если у вас есть одна из этих мутаций, это становится шансом на 10, 20 или даже 50 процентов».
В своей недавно опубликованной статье авторы SCHEMA отметили: «В одном из крупнейших на сегодняшний день исследований по секвенированию экзома мы идентифицировали гены, в которых варианты деструктивного кодирования придают значительный риск шизофрении в масштабе всего экзома. Эти усилия потребовали повторной обработки данных о последовательностях за десятилетие, гармонизации определения вариантов и контроля качества, включения внешних средств контроля и интеграции PTV [вариантов с усечением белка], повреждающих миссенс-варианты и варианты de novo. Подобные глобальные совместные усилия обеспечивают шаблон для борьбы с генетическим вкладом в другие сложные заболевания».
Подобные глобальные совместные усилия обеспечивают шаблон для борьбы с генетическим вкладом в другие сложные заболевания».
Нил далее прокомментировал: «Идентификация этих 10 генов является переломным моментом в исследованиях шизофрении, потому что каждый из них обеспечивает прочную основу для запуска биологических исследований. Секвенируя ДНК тысяч людей, мы начинаем точно понимать, какие гены имеют значение. Эти открытия являются отправной точкой для разработки новых методов лечения, которые лечат первопричину этого разрушительного состояния».
«В течение многих лет мы пытались добиться такого рода поддержки в биологии шизофрении», — сказал доктор философии Стивен Хайман, член института Broad core и директор Стэнли-центра. «В реальности потребуется еще несколько лет, чтобы преобразовать эти результаты в биомаркеры и методы лечения, которые изменят жизнь людей, страдающих от этой разрушительной болезни. Но это очень мотивирует, чтобы иметь убедительный путь вперед».
«В этих исследованиях представлены данные за 10 лет», — добавила Шинейд Чепмен, доктор философии, директор по управлению глобальными генетическими проектами в Центре Стэнли, которая вместе с членами команды Кристин Стивенс, Кэролайн Кьюсик и многими другими потратила сотни часов, гарантируя, что образцы и данные от сотрудников SCHEMA были должным образом обработаны и отслежены для этих анализов. «Это был довольно ручной процесс, поскольку не существует единой волшебной системы для соединения всех образцов и данных, а также всей связанной с ними нормативной и клинической информации».
«Это был довольно ручной процесс, поскольку не существует единой волшебной системы для соединения всех образцов и данных, а также всей связанной с ними нормативной и клинической информации».
Результаты исследования SCHEMA также указывают на дополнительные 22 гена, которые также, вероятно, влияют на риск шизофрении и могут оказаться значительными после дальнейшего изучения. Данные исследования SCHEMA доступны на schema.broadinstitute.org.
Вместе идентифицированные гены указывают на дисфункцию синапсов, где нейроны соединяются и взаимодействуют друг с другом, как на возможную причину шизофрении. Эта идея впервые возникла несколько лет назад, отчасти благодаря исследованию 2016 года, проведенному исследователями из Центра Стэнли Броуда, Гарвардской медицинской школы и Бостонской детской больницы. В этом исследовании исследователи впервые описали, как вариации в одном гене — компоненте комплемента 4 или С4 — повышают риск шизофрении, вызывая чрезмерную «обрезку» синапсов.
Информация о двух из 10 генов из исследования SCHEMA, GRIN2A и GRIA3 , также указывает на то, что синапс является ключевой частью механистических корней шизофрении. Эти два гена кодируют части рецептора глутамата, клеточной антенны, обнаруженной в синапсе, которая позволяет нейронам получать химические сигналы от соседних нейронов. Фармакологические исследования ранее предполагали, что передача сигналов глутамата может быть вовлечена в шизофрению, но исследование SCHEMA предоставляет первые убедительные генетические доказательства этого. Кроме того, GRIN2A активность мозга достигает пика в подростковом возрасте, примерно в то время, когда у людей, страдающих шизофренией, начинают проявляться симптомы.
«Полногеномный анализ резюмировал известные биологические процессы и вновь подтвердил, что гены риска шизофрении вовлечены в постсинаптическую плотность и более широкую синаптическую функцию и обогащены экспрессией в нейронных тканях», — прокомментировали авторы SCHEMA в своем отчете. «Связь PTV в субъединице рецептора NMDA GRIN2A с риском шизофрении обеспечивает генетическую поддержку нарушения регуляции глутаматергической передачи сигналов как возможного механизма заболевания».
«Связь PTV в субъединице рецептора NMDA GRIN2A с риском шизофрении обеспечивает генетическую поддержку нарушения регуляции глутаматергической передачи сигналов как возможного механизма заболевания».
Большинство генов SCHEMA никогда ранее не ассоциировались с мозговым расстройством или специфическими функциями нейронов. Один ген ( SETD1A ) участвует в регуляции транскрипции. Другой ( CUL1 ) помогает клетке перерабатывать старые или ненужные белки, а еще один ( XPO7 ) помогает молекулам-шаперонам выходить из ядра клетки. Тем не менее, согласно анализу SCHEMA, PTV в этих генах приводят к 20–52-кратному увеличению риска шизофрении.
«У нас еще нет хорошо разработанной основы для понимания того, как эти гены могут играть роль в шизофрении», — сказал соавтор SCHEMA и сотрудник PGC Марк Дейли, доктор философии, который также является членом института Стэнли. Центр Массачусетского государственного факультета АТГУ и директор Института молекулярной медицины, Финляндия. «Эти гены в конечном итоге приведут к некоторым новым открытиям, но потребуют много экспериментальных исследований, чтобы увидеть, какое место они могут вписать в головоломку».
«Эти гены в конечном итоге приведут к некоторым новым открытиям, но потребуют много экспериментальных исследований, чтобы увидеть, какое место они могут вписать в головоломку».
Команда PGC под руководством ученых из Университета Кардиффа изучила общие генетические вариации у 76 755 человек с шизофренией и у 243 649 человек без этого расстройства, обнаружив, что 287 локусов генома в некоторой степени связаны с риском шизофрении, что на 94 локуса больше, чем в последнем анализе PGC. был выпущен в 2019 году. При дальнейшем анализе группы PGC выявили 120 генов, которые потенциально повышают риск шизофрении. Некоторые из этих генов также были идентифицированы в исследовании SCHEMA.
Кроме того, результаты PGC показали, что генетический риск шизофрении наблюдается в генах, сконцентрированных в клетках мозга, называемых нейронами, но не в какой-либо другой ткани или типе клеток, что позволяет предположить, что биологическая роль этих клеток имеет решающее значение при шизофрении.
«Предыдущие исследования показали связь между шизофренией и многими анонимными последовательностями ДНК, но редко удавалось связать результаты с конкретными генами», — сказал соавтор, профессор Майкл О’Донован, доктор философии, из отдела психологической медицины. и клиническая неврология в Кардиффском университете.
«Настоящее исследование не только значительно увеличило количество этих ассоциаций, но теперь мы смогли связать многие из них с конкретными генами, что является необходимым шагом на трудном пути к пониманию причин этого расстройства и выявлению новых лечения».
Помимо того, что это крупнейшее исследование в своем роде, исследователь PGC включил более 7000 человек афроамериканского или латиноамериканского происхождения в то, что, по словам команды, является небольшим шагом к тому, чтобы достижения, полученные в результате генетических исследований, могли принести пользу людям за пределами лица европейского происхождения.
Хотя существует большое количество генетических вариантов, связанных с шизофренией, исследование показало, что они сконцентрированы в генах, экспрессируемых в нейронах, что указывает на эти клетки как на наиболее важный участок патологии. Результаты также показали, что аномальная функция нейронов при шизофрении затрагивает многие области мозга, что может объяснить ее разнообразные симптомы, которые могут включать галлюцинации, бред и проблемы с ясным мышлением. «Мы показываем, что гены, которым мы отдаем приоритет в ассоциированных локусах с помощью точного картирования, обогащены генами с повышенным бременем редких вредных мутаций при шизофрении, и идентифицируем GRIN2A, SP4, STAG1 и FAM120A как специфические гены, в которых конвергенция редких и распространенных вариантов ассоциации решительно поддерживают их патогенную роль в расстройстве», — написала команда PGC в опубликованной статье. «Обогащение общих вариантов ассоциаций было ограничено генами, которые экспрессируются в нейронах центральной нервной системы — как возбуждающими, так и тормозными — и которые выполняют функции в фундаментальных биологических процессах, связанных с функцией нейронов. Это указывает на то, что нейроны являются наиболее важным местом патологии при шизофрении».
Результаты также показали, что аномальная функция нейронов при шизофрении затрагивает многие области мозга, что может объяснить ее разнообразные симптомы, которые могут включать галлюцинации, бред и проблемы с ясным мышлением. «Мы показываем, что гены, которым мы отдаем приоритет в ассоциированных локусах с помощью точного картирования, обогащены генами с повышенным бременем редких вредных мутаций при шизофрении, и идентифицируем GRIN2A, SP4, STAG1 и FAM120A как специфические гены, в которых конвергенция редких и распространенных вариантов ассоциации решительно поддерживают их патогенную роль в расстройстве», — написала команда PGC в опубликованной статье. «Обогащение общих вариантов ассоциаций было ограничено генами, которые экспрессируются в нейронах центральной нервной системы — как возбуждающими, так и тормозными — и которые выполняют функции в фундаментальных биологических процессах, связанных с функцией нейронов. Это указывает на то, что нейроны являются наиболее важным местом патологии при шизофрении».
Профессор Джеймс Уолтерс, соавтор статьи, подготовленной Кардиффом, и директор Центра нейропсихиатрической генетики и геномики MRC в Университете Кардиффа, сказал: «Хотя люди с шизофренией могут выздороветь, многие плохо реагируют на лечение, испытывают долгосрочные проблемы с их психическим и физическим здоровьем, а также влияние на отношения, образование и работу. Мы надеемся, что результаты этого и сопутствующих исследований могут быть использованы для улучшения нашего понимания расстройства и облегчения разработки радикально новых лечения. Однако эти процессы часто бывают непростыми, и требуется много работы других нейробиологов, чтобы преобразовать генетические данные в детальное понимание механизмов болезни».
Консорциум психиатрической геномики финансируется Национальным институтом психического здоровья (NIMH), а работа в Кардиффе дополнительно поддерживалась Советом по медицинским исследованиям. Джошуа Гордон, директор NIMH, сказал: «Эти результаты, достигнутые благодаря беспрецедентному по своим масштабам глобальному сотрудничеству, знаменуют собой важный шаг вперед в нашем понимании происхождения шизофрении. Полученные данные позволят исследователям сосредоточиться на конкретных путях мозга в продолжающейся охоте за новыми методами лечения этого серьезного психического заболевания».
Полученные данные позволят исследователям сосредоточиться на конкретных путях мозга в продолжающейся охоте за новыми методами лечения этого серьезного психического заболевания».
Исследование PGC продемонстрировало важность и силу больших выборок в генетических исследованиях для понимания психических расстройств. В настоящее время команда стремится привлечь больше участников исследования и создать более крупные и разнообразные наборы данных, чтобы еще больше углубить наше понимание шизофрении.
Природа и эффект вариантов, обнаруженных PGC, в некоторых отношениях отличались от результатов SCHEMA, отметил Институт Броуда. Например, кодирующий повреждающий белок GRIN2A 9Мутации 0048, выявленные SCHEMA, встречаются крайне редко и повышают риск шизофрении в 24 раза. Варианты, обнаруженные в исследовании PGC, встречаются гораздо чаще и изменяют экспрессию GRIN2A , увеличивая риск всего в 1,06 раза.
Однако тот факт, что результаты обоих исследований объединяют сходные группы генов и сходные биологические механизмы, предполагает, что генетические открытия начинают концентрироваться на основных аспектах биологии шизофрении и приближаются к более широкому пониманию механизмов, лежащих в основе прогрессирования шизофрении.
Большинство генов SCHEMA никогда ранее не ассоциировались с мозговым расстройством или специфическими функциями нейронов. Один ген ( SETD1A ) участвует в регуляции транскрипции. Другой (CUL1) помогает клетке перерабатывать старые или ненужные белки, а еще один ( XPO7 ) помогает молекулам-шаперонам выходить из ядра клетки. Тем не менее, согласно анализу SCHEMA, PTV в этих генах приводят к 20–52-кратному увеличению риска шизофрении.
«У нас еще нет хорошо разработанной основы для понимания того, как эти гены могут играть роль в шизофрении», — сказал соавтор SCHEMA и сотрудник PGC Марк Дейли, доктор философии, который также является членом института Стэнли. Центр Массачусетского технологического факультета АТГУ и директор Института молекулярной медицины, Финляндия. «Эти гены в конечном итоге приведут к некоторым новым открытиям, но потребуют много экспериментальных исследований, чтобы увидеть, какое место они могут вписать в головоломку».
Команда PGC под руководством ученых из Университета Кардиффа изучила общие генетические вариации у 76 755 человек с шизофренией и у 243 649 человек без этого расстройства, обнаружив, что 287 локусов генома в некоторой степени связаны с риском шизофрении, что на 94 локуса больше, чем в последнем анализе PGC. был выпущен в 2019 году. При дальнейшем анализе группы PGC выявили 120 генов, которые потенциально повышают риск шизофрении. Некоторые из этих генов также были идентифицированы в исследовании SCHEMA.
был выпущен в 2019 году. При дальнейшем анализе группы PGC выявили 120 генов, которые потенциально повышают риск шизофрении. Некоторые из этих генов также были идентифицированы в исследовании SCHEMA.
Кроме того, результаты PGC показали, что генетический риск шизофрении наблюдается в генах, сконцентрированных в клетках мозга, называемых нейронами, но не в какой-либо другой ткани или типе клеток, что позволяет предположить, что биологическая роль этих клеток имеет решающее значение при шизофрении.
«Предыдущие исследования показали связь между шизофренией и многими анонимными последовательностями ДНК, но редко удавалось связать результаты с конкретными генами», — сказал соавтор, профессор Майкл О’Донован, доктор философии, из отдела психологической медицины. и клиническая неврология в Кардиффском университете.
«Настоящее исследование не только значительно увеличило количество этих ассоциаций, но теперь мы смогли связать многие из них с конкретными генами, что является необходимым шагом на трудном пути к пониманию причин этого расстройства и выявлению новых лечения».
Помимо того, что это крупнейшее исследование в своем роде, исследователь PGC включил более 7000 человек афроамериканского или латиноамериканского происхождения в то, что, по словам команды, является небольшим шагом к тому, чтобы достижения, полученные в результате генетических исследований, могли принести пользу людям за пределами лица европейского происхождения.
Хотя существует большое количество генетических вариантов, связанных с шизофренией, исследование показало, что они сконцентрированы в генах, экспрессируемых в нейронах, что указывает на эти клетки как на наиболее важный участок патологии. Результаты также показали, что аномальная функция нейронов при шизофрении затрагивает многие области мозга, что может объяснить ее разнообразные симптомы, которые могут включать галлюцинации, бред и проблемы с ясным мышлением. «Мы показываем, что гены, которым мы отдаем приоритет в ассоциированных локусах с помощью точного картирования, обогащены генами с повышенным бременем редких вредных мутаций при шизофрении, и идентифицируем GRIN2A, SP4, STAG1 и FAM120A как специфические гены, в которых конвергенция редких и распространенных вариантов ассоциации решительно поддерживают их патогенную роль в расстройстве», — написала команда PGC в опубликованной статье. «Обогащение общих вариантов ассоциаций было ограничено генами, которые экспрессируются в нейронах центральной нервной системы — как возбуждающими, так и тормозными — и которые выполняют функции в фундаментальных биологических процессах, связанных с функцией нейронов. Это указывает на то, что нейроны являются наиболее важным местом патологии при шизофрении».
«Обогащение общих вариантов ассоциаций было ограничено генами, которые экспрессируются в нейронах центральной нервной системы — как возбуждающими, так и тормозными — и которые выполняют функции в фундаментальных биологических процессах, связанных с функцией нейронов. Это указывает на то, что нейроны являются наиболее важным местом патологии при шизофрении».
Профессор Джеймс Уолтерс, соавтор статьи, подготовленной Кардиффом, и директор Центра нейропсихиатрической генетики и геномики MRC в Университете Кардиффа, сказал: «Хотя люди с шизофренией могут выздороветь, многие плохо реагируют на лечение, испытывают долгосрочные проблемы с их психическим и физическим здоровьем, а также влияние на отношения, образование и работу. Мы надеемся, что результаты этого и сопутствующих исследований могут быть использованы для улучшения нашего понимания расстройства и облегчения разработки радикально новых лечения. Однако эти процессы часто бывают непростыми, и требуется много работы других нейробиологов, чтобы преобразовать генетические данные в детальное понимание механизмов болезни».
Консорциум психиатрической геномики финансируется Национальным институтом психического здоровья (NIMH), а работа в Кардиффе дополнительно поддерживалась Советом по медицинским исследованиям. Джошуа Гордон, директор NIMH, сказал: «Эти результаты, достигнутые благодаря беспрецедентному по своим масштабам глобальному сотрудничеству, знаменуют собой важный шаг вперед в нашем понимании происхождения шизофрении. Полученные данные позволят исследователям сосредоточиться на конкретных путях мозга в продолжающейся охоте за новыми методами лечения этого серьезного психического заболевания».
Исследование PGC продемонстрировало важность и силу больших выборок в генетических исследованиях для понимания психических расстройств. В настоящее время команда стремится привлечь больше участников исследования и создать более крупные и разнообразные наборы данных, чтобы еще больше углубить наше понимание шизофрении.
Природа и эффект вариантов, обнаруженных PGC, в некоторых отношениях отличались от результатов SCHEMA, отметил Институт Броуда. Например, кодирующий повреждающий белок GRIN2A 9Мутации 0048, выявленные SCHEMA, встречаются крайне редко и повышают риск шизофрении в 24 раза. Варианты, обнаруженные в исследовании PGC, встречаются гораздо чаще и изменяют экспрессию GRIN2A , увеличивая риск всего в 1,06 раза.
Например, кодирующий повреждающий белок GRIN2A 9Мутации 0048, выявленные SCHEMA, встречаются крайне редко и повышают риск шизофрении в 24 раза. Варианты, обнаруженные в исследовании PGC, встречаются гораздо чаще и изменяют экспрессию GRIN2A , увеличивая риск всего в 1,06 раза.
Однако тот факт, что результаты обоих исследований объединяют сходные группы генов и сходные биологические механизмы, предполагает, что генетические открытия начинают концентрироваться на основных аспектах биологии шизофрении и приближаются к более широкому пониманию механизмов, лежащих в основе прогрессирования шизофрении.
«Мы надеялись, что в конечном итоге мы получим некоторое совпадение в историях, которые рассказывали нам общие и редкие варианты ассоциаций», — сказал Нил. «И мы видим совпадение, указывающее на связь между синаптической биологией и риском шизофрении». Хотя, как отмечают исследователи PGC в своей статье, «нарушение функции нейронов при шизофрении вряд ли ограничивается синапсом, концентрация ассоциаций в генах с пре- и постсинаптической локализацией, а также с функциями, связанными с синаптической организацией, дифференцировкой и передачи, указывают на патофизиологическое значение этих нейронных компартментов и сопутствующих им функций».
Данные SCHEMA также проливают свет на то, как психические расстройства и расстройства развития нервной системы в более широком смысле могут иметь общий генетический риск. Например, несколько генов SCHEMA, в том числе GRIN2A , ранее были связаны с нарушениями развития нервной системы, такими как эпилепсия, задержка развития и умственная отсталость.
Но, сравнивая свои данные с данными других крупномасштабных исследований, команда SCHEMA отметила, что наблюдаемые ими совпадения были вызваны различными видами мутаций: PTV для шизофрении, миссенс-мутациями (которые могут привести к заменам аминокислот, которые модифицируют активность белка) при нарушениях развития нервной системы.
«Мы видим, что различные виды мутаций в одних и тех же генах могут вызывать самые разные последствия, — отметил Нил. «Нам предстоит еще многое сделать и узнать о том, что делают эти гены, что делают вариации этих генов и каковы биологические последствия генетической изменчивости на самом деле».
«Этот момент имеет решающее значение для понимания того, как работает генетика при заболеваниях головного мозга», — добавил Дейли. «Мы должны убедиться, что мы не изолируем эти данные, а вместо этого остаемся открытыми для изучения того, чему эта генетика может научить нас по фенотипам».
«Эти первые 10 генов — на самом деле только начало генетических открытий, — сказал Нил. «Есть довольно четкие доказательства того, что существует гораздо больше генов, которые можно открыть, используя тот же подход. Но нам принципиально нужны большие размеры выборки, чтобы иметь возможность выявить эти дополнительные гены.
«Но если у вас есть больше кусочков головоломки, — продолжил он, — может быть, будет немного легче собрать их вместе и прийти к более последовательному механистическому взгляду на шизофрению, и как мы могли бы начать подходить к этим процессов с надеждой на улучшение жизни пациентов».
«Биологическая сложность шизофрении действительно пугает, но эта комбинация редких вариантов, изменяющих белок, полученных в результате секвенирования экзома, и распространенных вариантов, полученных в ходе GWAS, позволила нам понять корни этой сложности», — сказал Хайман.