Когнитивный резерв, когнитивные нарушения и возможность их медикаментозной коррекции
Одной из наиболее серьезных медико-социальных проблем на сегодняшний день является проблема деменции. Это связано с целым рядом причин, в частности с ростом продолжительности жизни, увеличением в популяции доли лиц пожилого и старческого возраста, изменением особенностей образа жизни, включая характер и объем физических и эмоциональных нагрузок, рациона питания, воздействия целого ряда химических факторов, повышением качества диагностики и совершенствованием методов выявления когнитивных нарушений. Исключительная важность проблемы обусловлена и большими материальными расходами, которые связаны не только с лечением пациента с деменцией, но и с осуществлением мероприятий по обеспечению его жизнедеятельности, ухода за ним.
Материальные затраты на пациентов с деменцией исключительно высоки и демонстрируют неуклонную тенденцию к дальнейшему нарастанию. Так, в США в последнюю декаду ХХ века они возросли втрое и вдвое они могут возрасти к 2030 г.
Наблюдается зависимость нарастания частоты деменции с возрастом. Так, деменция выявляется у 5% лиц старше 65 лет, тогда как среди лиц старше 85 лет она выявляется уже у 50% населения [5]. В Российской Федерации при относительно невысокой средней продолжительности жизни доля пожилых в обществе также неуклонно увеличивается [6].
Важнейшими причинами развития деменции являются болезнь Альцгеймера (БА), сосудистые поражения головного мозга, нейродегенеративные заболевания (болезнь Паркинсона, деменция с тельцами Леви, болезнь Гентингтона и др.
В качестве одного из факторов, потенциально способных замедлить наступление деменции и сделать ее течение более мягким, большой практический и теоретический интерес представляет концепция когнитивного резерва (КР) [7, 8]. В соответствии с данной концепцией, вероятность развития деменции определяют врожденные структурно-функциональные особенности головного мозга, а также такие приобретенные факторы, как уровень образования и интеллектуальных нагрузок в течение жизни, характер трудовой деятельности и стиль проведения досуга. Ранее предполагалось, что наиболее значимым для последующего развития интеллекта индивидуума является полученный в раннем детстве опыт [9], однако последующие исследования показали, что важный вклад в формирование КР вносит поддержание интеллектуальной деятельности в течение последующей жизни [10]. Более высокий уровень испытываемых индивидуумом в течение жизни интеллектуальных нагрузок и высокий уровень образования связаны с меньшей вероятностью развития когнитивных расстройств в последующем.
На состояние КР оказывают влияние образ социального поведения, положение индивидуума в социальной иерархии, хотя результаты таких исследований носят неоднозначный характер. Так, изначально более высокий уровень интеллектуального развития и более активное социальное поведение, связанное с трудовой деятельность и проведением досуга, способствуют большей сохранности когнитивных функций в пожилом возрасте [11]. Некоторые исследователи [12] считают, что более высокий исходный уровень КР, особенности образа жизни и социально-экономическое положение способны оказывать превентивное действие в отношении развития БА и возрастного когнитивного снижения. Одним из факторов, обеспечивающих формирование и поддержание высокого уровня КР, является также билингвизм [13], делающий возможным переключение с одного языка на другой в процессе общения и построении грамматически правильных фраз, что требует высокоэффективных процессов контроля. Сказанное подтверждается наблюдениями, что многие нейропсихологические тесты намного лучше выполняются владеющими двумя языками взрослыми и пожилыми лицами, чем их ровесниками, владеющими только одним языком.
Однако предшествующий развитию заболевания КР не всегда в полной мере способен оказать свое протективное действие. Так, A. Singh-Manoux и соавт. [14] при наблюдении за 8000 государственных служащих Лондона (средний возраст 56±6 лет), установили, что уровень КР коррелировал с исходным уровнем когнитивных функций, при этом наиболее сильная корреляционная связь имелась с занимаемой должностью. Вместе с тем выраженность когнитивного снижения к окончанию периода наблюдения оказалась максимальной у лиц, занимавших наиболее высокие административные должности. Метаанализ значительного числа клинических исследований (в них было включено более 29 000 обследованных) показал, что высокий исходный уровень КР ассоциирован с 50% снижения риска развития деменции в последующем [15].
Подтверждение защитной роли КР в отношении развития деменции было получено N. Scarmeas и соавт. [10] при изучении состояния мозгового кровотока методом позитронно-эмиссионной томографии (ПЭТ) у пациентов с БА (снижение мозгового кровотока является косвенным маркером, подтверждающим выраженность структурных изменений вещества головного мозга при нейродегенеративном процессе [16]).
Можно выделить активный и пассивный механизмы формирования КР. Пассивный включает такие структурные характеристики мозга, как его объем, количество функционирующих синапсов, обладающих буферными функциями по отношению к повреждению [18].
Одним из механизмов защитных эффектов КР в условиях старения является реорганизация некоторых церебральных структур, ответственных за выполнение тех или иных функций, в частности речевых [19]. В зависимости от выполняемых задач наблюдается перераспределение активности между полушариями, а также между передними и задними отделами головного мозга. Благодаря этому обеспечивается оптимизация выполнения когнитивных функций, что делает возможным эффективное выполнение различных видов деятельности даже в условиях структурного поражения мозгового вещества вследствие старения.
Имеются морфологические подтверждения роли КР в предупреждении когнитивных нарушений. Так, при исследовании аутопсийного мозга пациентов, у которых при жизни отсутствовали когнитивные нарушения, в ряде случаев выявлялись различной степени выраженности изменения, характерные для БА [20]. Интересны прижизненные исследования C. Wiley и соавт. [21], проведенные на основании оценки интенсивности накопления в ткани головного мозга специфического маркера, позволяющего визуализировать амилоидные накопления при БА. Речь идет о питтсбургском соединении В (Pittsburgh compound B), выявляемом при помощи ПЭТ. Было установлено, что его максимальное накопление отмечается на развернутых стадиях БА, при этом его количество коррелирует с грубым когнитивным дефицитом. Однако D. Rentz и соавт. [22] показали, что такая зависимость характерна для пациентов с относительно низким КР, при более высоком его уровне, несмотря на обильные отложения амилоида, когнитивные функции остаются более сохранными.
Практическая значимость концепции КР состоит в том, что его использование позволяет планировать стратегии индивидуальной профилактики развития деменции с использованием различных лекарственных и немедикаментозных воздействий. В ряде клинических исследований [23, 24], посвященных изучению данной проблемы, было показано, что когнитивные тренировки различной модальности способны не только замедлить развитие когнитивного снижения у пожилых людей, но и улучшить их мыслительные способности. Как свидетельствуют результаты одного из масштабных пятилетних исследований [25], в которое были включены 2800 пациентов, проходивших систематический тренинг, направленный на улучшение когнитивных функций, положительный эффект сохранялся на протяжении всего периода исследования.
В ряде клинических исследований [23, 24], посвященных изучению данной проблемы, было показано, что когнитивные тренировки различной модальности способны не только замедлить развитие когнитивного снижения у пожилых людей, но и улучшить их мыслительные способности. Как свидетельствуют результаты одного из масштабных пятилетних исследований [25], в которое были включены 2800 пациентов, проходивших систематический тренинг, направленный на улучшение когнитивных функций, положительный эффект сохранялся на протяжении всего периода исследования.
Роль КР в предупреждении развития тяжелой деменции и замедления темпов когнитивного снижения не исключает применения адекватно подобранной медикаментозной терапии. Ее выбор определяется представлениями о патогенетических механизмах развития деменции.
В настоящее время достаточно подробно изучены молекулярные и клеточные механизмы развития деменции как при нейродегенеративных заболеваниях, в частности, при БА, так и при сосудистом поражении головного мозга.

Избыточная активность глутамат- и аспартатергической нейротрансмиссии связана с целым рядом негативных эффектов. Считается, что чрезмерная, в том числе длительная активация соответствующих рецепторов, ведет к избыточному возбуждению постсинаптических нейронов, неадекватному притоку ионов кальция в нервные клетки по рецептор-ассоциированным ионным каналам и ряду других негативных последствий [28]. Итогом этих процессов является повреждение и гибель нейронов, что было убедительно продемонстрировано на моделях повреждения головного мозга (острая ишемия, травма, нейродегенерация и др.), а также в клинических условиях [29]. Показана возможность отсроченной гибели нейронов, в частности, по механизму апоптоза, вследствие эксайтотоксичности, а также потенциально обратимое нарушение их функции, которое может рассматриваться в качестве объекта терапевтического вмешательства.
Предпринимались попытки фармакологической регуляции глутаматергической нейротрансмиссии, ряд из которых окончился неудачно из-за того, что значительное ее угнетение приводило к расстройствам сознания, поведения, нарастанию когнитивных нарушений [30, 31]. Вследствие этого некоторые лекарственные препараты, оказывавшие определенный эффект в условиях эксперимента, не получили применения в клинической практике.
Вследствие этого некоторые лекарственные препараты, оказывавшие определенный эффект в условиях эксперимента, не получили применения в клинической практике.
В связи со сказанным значительный интерес представляет мемантин, новой торговой маркой которого является препарат меманталь. В результате проведенных фармакологических исследований была подтверждена полная биоэквивалентность меманталя оригинальному препарату.
Мемантин (меманталь) является умеренно аффинным неконкурентным антагонистом потенциалзависимых НМДА-рецепторов. Исключительно важной его особенностью является то, что он способен предохранять нейроны от повреждения в условиях избыточного выброса глутамата в синаптическую щель [32, 33]. В то же время, принципиальным отличием от многих изучавшихся антагонистов глутаматных рецепторов, особенность мемантина заключается в том, что при его назначении отсутствует угнетение нейротрансмиссии в нормально функционирующих синапсах, вследствие чего применение в терапевтических дозировках не сопровождается расстройствами сознания и когнитивными нарушениями.
В экспериментальных исследованиях была установлена эффективность мемантина как в культурах нервной ткани, так и в моделях дегенеративного поражения мозгового вещества у животных.
Очередным этапом изучения препарата явилось проведение рандомизированных клинических исследований в тщательно отобранных группах пациентов. Одним из них является исследование I. Aprahamian и соавт. [34], касавшиеся пациентов с БА. Полученные в таких работах результаты были неоднократно проанализированы, о чем свидетельствуют ряд опубликованных метаанализов и систематизированных обзоров.
Серьезной проблемой в терапии заболеваний, приводящих к деменции, является возможность ее раннего распознавания. Было показано [35], что выявление пациентов на преддементной стадии способно обеспечить своевременное начало лечения и соответственно относительно более благоприятный исход заболевания. Вместе с тем вопрос о том, насколько эффективны такие мероприятия в масштабах популяции, в частности как велика значимость скрининга и других способов раннего выявления когнитивных нарушений и насколько они способны предотвратить развитие деменции, остается открытым [36].
Опубликованы результаты многочисленных рандомизированных клинических исследований [37-39], в которых были получены достаточно убедительные данные в отношении высокой эффективности мемантина при деменции у пациентов с БА. Накоплен отечественный опыт применения мемантина при БА смешанной деменции и деменции с тельцами Леви [40]. Установлено, что наиболее выраженным и стойким эффект оказался у больных с АД и смешанной деменцией. Положительный эффект заключался преимущественно в уменьшении выраженности модально-неспецифических нарушений памяти, улучшении способности к обобщению, выстраиванию программы действия и контролю за выполняемыми операциями; было отмечено замедление когнитивного снижения в процессе терапии. Более стабильный эффект наблюдался при длительном приеме препарата.
Предпринимались попытки оценки эффективности применения мемантина в зависимости от выраженности когнитивных нарушений на момент начала терапии. Так, проведенный в Швеции метаанализ [41] был основан на результатах 6 рандомизированных исследований, в которые были включены 1826 пациентов с умеренно выраженной и тяжелой деменцией (по MMSE не более 20 баллов) при БА. Был сделать вывод о том, что применение мемантина при достаточно длительном сроке обеспечивает не только улучшение мнестических функций и способности к обучению, повышение эффективности выполнения ряда психометрических тестов, но и расширение способности к самообслуживанию и повышению качества жизни больных [49].
Был сделать вывод о том, что применение мемантина при достаточно длительном сроке обеспечивает не только улучшение мнестических функций и способности к обучению, повышение эффективности выполнения ряда психометрических тестов, но и расширение способности к самообслуживанию и повышению качества жизни больных [49].
Проводилось также изучение эффективности мемантина у пациентов с менее выраженными когнитивными нарушениями вследствие БА (по MMSE от 20 до 23 баллов). В одном из предварительных рандомизированнных исследований [42] были получены достаточно обнадеживающие результаты, в частности, при лечении больных, получавших мемантин на протяжении 24 нед. Но менее убедительными оказались результаты проведенного в последующем метаанализа [43]: не было установлено положительного эффекта проводимой терапии в виде улучшения когнитивных функций или замедления их снижения. Тем не менее результаты приведенных выше и других рандомизированных контролируемых исследований явились основанием для рекомендаций в отношении применения мемантина пациентам с умеренно выраженной и тяжелой деменцией при БА в странах Европейского Союза (2002) и США (2003) [43].
Целый ряд последующих исследований был посвящен анализу эффективности мемантина у пациентов не только с БА, но и другими формами деменции. Результаты рандомизированных исследований, посвященных оценке лечения пациентов с различными типами деменции (БА, сосудистая деменция, деменция смешанного типа и др.), были повторно проанализированы в систематизированных обзорах [43]. Их авторы отметили, что применение мемантина эффективно у пациентов с различными типами деменции, более выраженный эффект наблюдается при использовании высоких доз препарата (20 мг в сутки) на протяжении достаточного периода времени (6 нед и более). Отмечена хорошая переносимость препарата даже при длительном лечении. Из побочных эффектов зарегистрированы эпизоды психомоторного возбуждения у отдельных пациентов [45].
Активно изучалась возможность назначения мемантина у больных с деменцией с тельцами Леви [46], что нашло отражение в метаанализе таких исследований, которые позволили установить, что при этом заболевании проведенное лечение оказалось менее эффективным, чем у пациентов с БА, хотя по ряду оцениваемых параметров мемантин был эффективнее плацебо. Кроме того, авторы констатировали хорошую переносимость терапии и незначительное число побочных явлений.
Кроме того, авторы констатировали хорошую переносимость терапии и незначительное число побочных явлений.
Сопоставимые результаты были получены и в ходе другого исследования [47], в котором пациенты с легкой и умеренной деменцией вследствие болезни Паркинсона и деменции с тельцами Леви получали мемантин по 20 мг в сутки на протяжении 24 нед. Авторы отметили улучшение в соответствии с оценкой состояния по шкале CGI, тогда как по другим шкалам существенного улучшения зарегистрировано не было. Было высказано предположение [48], что положительный эффект препарата при смешанных деменциях может быть обусловлен угнетением специфических для БА патогенетических механизмов развития заболевания. Интерес представляет тот факт, что мемантин не только обеспечивает стабилизацию или улучшение состояния когнитивных функций у больных болезнью Паркинсона и деменцией с тельцами Леви, но и обеспечивает повышение качества их жизни и расширение способности к самообслуживанию [49].
Таким образом, полученные к настоящему времени результаты применения мемантина свидетельствую о том, что его он оказывает положительный эффект при разных типах деменции, что позволяет рассматривать его как противодементный препарат с достаточно широким спектром действия, применение которого целесообразно и у пациентов с неустановленной и смешанной этиологией, в частности при сочетании БА с деменциями другого генеза [32]. Перспективным в этом отношении представляется применение препарата меманталь, эффективность которого продемонстрирована и доказана в ряде клинических исследований.
Перспективным в этом отношении представляется применение препарата меманталь, эффективность которого продемонстрирована и доказана в ряде клинических исследований.
Когнитивный резерв при рассеянном склерозе | Пашковская
1. Benedict R.H.B., Zivadinov R. Risk factors for and management of cognitive dysfunction in multiple sclerosis. Nat. Rev. Neurol. 2011;7(6): 332–342. https://doi.org/10.1038/nrneurol.2011.61
2. Sandroff B.M., Schwartz C.E., DeLuca J. Measurement and maintenance of reserve in multiple sclerosis. J. Neurol. 2016;263(11): 2158–2169. https://doi.org/10.1007/s00415-016-8104-5
3. Amato M.P., Hakiki B., Goretti B., Rossi F., Stromillo M.L., Giorgio A. et al. Italian RIS/MS Study Group. Association of MRI metrics and cognitive impairment in radiologically isolated syndromes. Neurology. 2012;78(5): 309–314. https://doi.org/10.1212/WNL.0b013e31824528c9
4. Planche V., Ruet A., Coupé P., Lamargue-Hamel D., Deloire M., Pereira B. et al. Hippocampal microstructural damage correlates with memory impairment in clinically isolated syndrome suggestive of multiple sclerosis.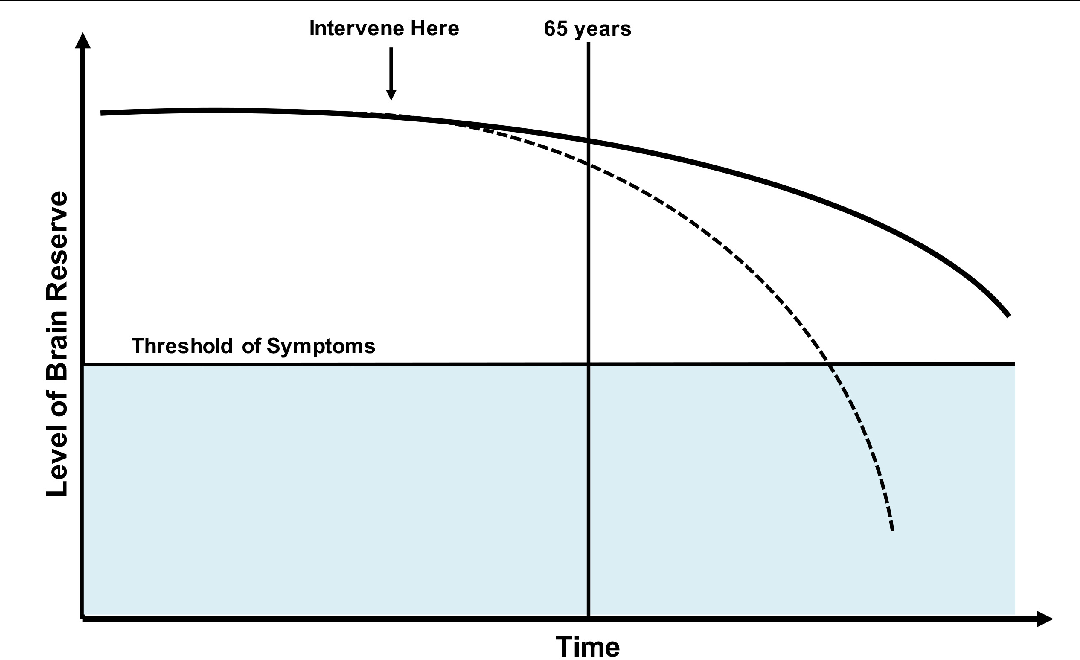 Mult. Scler. Houndmills Basingstoke Engl. 2017;23(9): 1214–1224. https://doi.org/10.1177/1352458516675750
Mult. Scler. Houndmills Basingstoke Engl. 2017;23(9): 1214–1224. https://doi.org/10.1177/1352458516675750
5. Ruano L., Portaccio E., Goretti B., Niccolai C., Severo M., Patti F. et al. Age and disability drive cognitive impairment in multiple sclerosis across disease subtypes. Mult. Scler. Houndmills Basingstoke Engl. 2017;23(9): 1258–1267. https://doi.org/10.1177/1352458516674367
6. Friese M.A., Schattling B., Fugger L. Mechanisms of neurodegeneration and axonal dysfunction in multiple sclerosis. Nat. Rev. Neurol. 2014;10(4): 225–238. https://doi.org/10.1038/nrneurol.2014.37
7. Patti F., Amato M.P., Trojano M., Bastianello S., Tola M.R., Goretti B. et al., COGIMUS Study Group. Cognitive impairment and its relation with disease measures in mildly disabled patients with relapsing-remitting multiple sclerosis: baseline results from the Cognitive Impairment in Multiple Sclerosis (COGIMUS) study. Mult. Scler. Houndmills Basingstoke Engl. 2009;15(7): 779–788. https://doi.org/10. 1177/1352458509105544
1177/1352458509105544
8. Ласков B.Б., Логачева Е.А., Третьякова Е.Е., Гриднев М.А. Клинико-эпидемиологические особенности больных рассеянным склерозом в Курской области. Неврология, нейропсихиатрия, психосоматика. 2017;9(1): 55–60. https://dx.doi.org/10.14412/2074-2711-2017-1-55-60
9. Langdon D.W. Cognition in multiple sclerosis. Curr. Opin. Neurol. 2011;24(3): 244–249. https://doi.org/10.1097/WCO.0b013e328346a43b
10. Katzman R., Aronson M., Fuld P., Kawas C., Brown T., Morgenstern H. et al. Development of dementing illnesses in an 80-yearold volunteer cohort. Ann. Neurol. 1989;25(4): 317–324. https://doi.org/10.1002/ana.410250402
11. Satz P. Brain reserve capacity on symptom onset after brain injury: A formulation and review of evidence for threshold theory. Neuropsychology. 1993;7(3): 273–295. https://doi.org/10.1037/0894-4105.7.3.273
12. Stern Y., Alexander G. E., Prohovnik I., Mayeux R. Inverse relationship between education and parietotemporal perfusion defi cit in Alzheimer’s disease. Ann. Neurol. 1992;32(3): 371–5. https://doi.org10.1002/ana.410320311
Ann. Neurol. 1992;32(3): 371–5. https://doi.org10.1002/ana.410320311
13. Quinn N.P., Rossor M.N., Marsden C D. Dementia and Parkinson’s disease-pathological and neurochemical considerations. Br. Med. Bull. 1986;42(1): 86–90. https://doi.org10.1093/oxfordjournals.bmb.a072104
14. Finnema S.J., Nabulsi N. B., Eid T., Detyniecki K., Lin S.-F., Chen M.-K. et al. Imaging synaptic density in the living human brain. Sci. Transl. Med. 2016;8:348ra96. https://doi.org/10.1126/scitranslmed.aaf6667
15. Коберская Н.Н., Табеева Г.Р. Современная концепция когнитивного резерва. Неврология, нейропсихиатрия, психосоматика. 2019;11(1): 96–102. https://doi.org/10.14412/2074-2711-2019-1-96-102
16. Еремина Д.А., Сидоровская Ю.М. Концепция когнитивного резерва в контексте изучения ишемической болезни сердца: современные представления и перспективы научных исследований. Вестник Российского университета дружбы народов. Серия: Психология и педагогика. 2019;16(1): 20–38. http://dx.doi.org/10. 22363/2313-1683-2019-16-1-20-38
22363/2313-1683-2019-16-1-20-38
17. Cabeza R., Albert M., Belleville S., Craik F., Duarte A., Grady C. et al. Maintenance, Reserve and Compensation: The Cognitive Neuroscience of Healthy Ageing. Nat. Rev. Neurosci. 2018;19(11): 701–710. https://doi.org/10.1038/s41583-018-0068-2
18. Ifantopoulou P., Artemiadis A. K., Bakirtzis C., Zekiou K., Papadopoulos T.-S., Diakogiannis I. et al. Cognitive and brain reserve in multiple sclerosis-A cross-sectional study. Mult. Scler. Relat. Disord. 2019;35: 128–134. https://doi.org/10.1016/j.msard.2019.07.027
19. Tiberio M., Chard D. T., Altmann D. R., Davies G., Griffin C. M., Rashid W. et al. Gray and White Matter Volume Changes in Early RRMS: A 2-Year Longitudinal Study. Neurology. 2005;64(6): 1001–1007. https://doi.org/10.1212/01.WNL.0000154526.22878.30
20. Sanfi lipo M. P., Benedict R. H. B., Sharma J., Weinstock-Guttman B., Bakshi R. The Relationship between Whole Brain Volume and Disability in Multiple Sclerosis: A Comparison of Normalized Gray vs. White Matter with Misclassifi cation Correction. NeuroImage. 2005;26(4): 1068–1077. https://doi.org/10.1016/j.neuroimage.2005.03.008
White Matter with Misclassifi cation Correction. NeuroImage. 2005;26(4): 1068–1077. https://doi.org/10.1016/j.neuroimage.2005.03.008
21. Fisniku L.K., Chard D.T., Jackson J.S., Anderson V.M., Altmann D.R., Miszkiel K.A. et al. Gray Matter Atrophy Is Related to Long-Term Disability in Multiple Sclerosis. Ann. Neurol. 2008;64(3): 247–254. https://doi.org/10.1002/ana.21423
22. Mesaros S., Rovaris M., Pagani E., Pulizzi A., Caputo D., Ghezzi A. et al. A Magnetic Resonance Imaging Voxel-Based Morphometry Study of Regional Gray Matter Atrophy in Patients with Benign Multiple Sclerosis. Arch. Neurol. 2008;65(9): 1223–1230. https://doi.org/10.1001/archneur.65.9.1223
23. Lucchinetti C.F., Popescu B.F.G., Bunyan R.F., Moll N.M., Roemer S.F., Lassmann H. et al. Infl ammatory Cortical Demyelination in Early Multiple Sclerosis. N. Engl. J. Med. 2011;365(23): 2188–2197. https://doi.org/10.1056/NEJMoa1100648
24. Medaglia J.D., Pasqualetti F., Hamilton R.H., Thompson-Schill S.L. , Bassett D.S. Brain and Cognitive Reserve: Translation via Network Control Theory. Neurosci. Biobehav. Rev. 2017;75: 53–64. https://doi.org/10.1016/j.neubiorev.2017.01.016
, Bassett D.S. Brain and Cognitive Reserve: Translation via Network Control Theory. Neurosci. Biobehav. Rev. 2017;75: 53–64. https://doi.org/10.1016/j.neubiorev.2017.01.016
25. van Loenhoud A.C., Groot C., Vogel J.W., van der Flier W.M., Ossenkoppele R. Is Intracranial Volume a Suitable Proxy for Brain Reserve? Alzheimers Res. Ther. 2018;10(1):91. https://doi.org/10.1186/s13195-018-0408-5
26. Artemiadis A., Bakirtzis C., Ifantopoulou P., Zis P., Bargiotas P., Grigoriadis N., Hadjigeorgiou G. The Role of Cognitive Reserve in Multiple Sclerosis: A Cross-Sectional Study in 526 Patients. Mult. Scler. Relat. Disord. 2020;41:102047. https://doi.org/10.1016/j.msard.2020.102047
27. Sumowski J.F., Rocca M.A., Leavitt V.M., Riccitelli G., Comi G., DeLuca J., Filippi M. Brain Reserve and Cognitive Reserve in Multiple Sclerosis: What You’ve Got and How You Use It. Neurology. 2013;80(24): 2186–2193. https://doi.org/10.1212/WNL.0b013e318296e98b
28. Sumowski J.F., Rocca M.A., Leavitt V. M., Dackovic J., Mesaros S., Drulovic J. et al. Brain Reserve and Cognitive Reserve Protect against Cognitive Decline over 4.5 Years in MS. Neurology. 2014;82(20): 1776–1783. https://doi.org/10.1212/WNL.0000000000000433
M., Dackovic J., Mesaros S., Drulovic J. et al. Brain Reserve and Cognitive Reserve Protect against Cognitive Decline over 4.5 Years in MS. Neurology. 2014;82(20): 1776–1783. https://doi.org/10.1212/WNL.0000000000000433
29. Живолупов C.А., Самарцев И.Н. Нейропластичность: патофизиологические аспекты и возможности терапевтической модуляции. Журнал неврологии и психиатрии им. С.С. Корсакова. 2009;109(4):78. URL: https://www.researchgate.net/publication/260368097
30. Nucci M., Mapelli D., Mondini S. Cognitive Reserve Index Questionnaire (CRIq): A New Instrument for Measuring Cognitive Reserve. Aging. Clin. Exp. Res. 2012;24(3): 218–226. https://doi.org/10.3275/7800
31. Kang J.M., Cho Y.-S., Park S., Lee B.H., Sohn B.K., Choi C.H. et al. Montreal Cognitive Assessment Refl ects Cognitive Reserve. BMC Geriatr. 2018;18(1):261. https://doi.org/10.1186/s12877-018-0951-8
32. Solé-Padullés C., Bartrés-Faz D., Junqué C., Vendrell P., Rami L., Clemente I.C. et al. Brain structure and function related to cognitive reserve variables in normal aging, mild cognitive impairment and Alzheimer’s disease. Neurobiol. Aging. 2009;30(7): 1114–1124. https://doi.org/10.1016/j.neurobiolaging.2007.10.008
Neurobiol. Aging. 2009;30(7): 1114–1124. https://doi.org/10.1016/j.neurobiolaging.2007.10.008
33. Дайникова Е.И., Пизова Н.В. Когнитивный резерв и когнитивные нарушения: лекарственные и нелекарственные методы коррекции. Неврология, нейропсихиатрия, психосоматика. 2014;(Спецвып.2): 62–68. http://dx.doi.org/10.14412/2074-2711-2014-2S-62-68
34. Литовченко А.И. Нарушения речи при опухолях мозжечка. Украинский нейрохирургический журнал. 2012;2:4–6. https://doi.org/616.22-008.5:616.831.71-006
35. Фокин В.Ф., Пономарева Н.В., Коновалов Р.Н., Кротенкова М.В., Медведев Р.Б., Лагода О.В., Танашян М.М. Изменения коннективности головного мозга у больных с нарушениями вербальной оперативной памяти при дисциркуляторной энцефалопатии. Вестник РГМУ. 2019;5. https://doi.org/10.24075/vrgmu.2019.061
36. Белопасова А.В., Кадыков А.С., Коновалов Р.Н., Кремнева Е.И. Организация нейрональной речевой системы у здоровых лиц и ее реорганизация у пациентов с постинсультной афазией. Анналы клинической и экспериментальной неврологии. 2013;7(1). URL: http://annalynevrologii.com/journal/index.php/pathID/article/view/24736. Solé-Padullés C., Bartrés-Faz D., Junqué C., Vendrell P., Rami L., Clemente I.C. et al. Brain structure and function related to cognitive reserve variables in normal aging, mild cognitive impairment and Alzheimer’s disease. Neurobiol. Aging. 2009;30(7):1114–1124. https://doi.org/10.1016/j.neurobiolaging.2007.10.008
2013;7(1). URL: http://annalynevrologii.com/journal/index.php/pathID/article/view/24736. Solé-Padullés C., Bartrés-Faz D., Junqué C., Vendrell P., Rami L., Clemente I.C. et al. Brain structure and function related to cognitive reserve variables in normal aging, mild cognitive impairment and Alzheimer’s disease. Neurobiol. Aging. 2009;30(7):1114–1124. https://doi.org/10.1016/j.neurobiolaging.2007.10.008
37. Paterson D.H., Warburton D.E. Physical activity and functional limitations in older adults: a systematic review related to Canada’s Physical Activity Guidelines. Int. J. Behav. Nutr. Phys. Act. 2010;7:38. https://doi.org/10.1186/1479-5868-7-38
38. Motl R.W., Dlugonski D., Pilutti L., Sandroff B., McAuley E. Premorbid Physical Activity Predicts Disability Progression in Relapsing- Remitting Multiple Sclerosis. J. Neurol. Sci. 2012;323(1– 2):123–127. https://doi.org/10.1016/j.jns.2012.08.033
39. Kurtzke J.F. Rating Neurologic Impairment in Multiple Sclerosis: An Expanded Disability Status Scale (EDSS). Neurology. 1983;33(11):1444–1452. https://doi.org/10.1212/wnl.33.11.1444
Neurology. 1983;33(11):1444–1452. https://doi.org/10.1212/wnl.33.11.1444
40. Scarmeas N., Stern Y. Cognitive reserve and lifestyle. J. Clin. Exp. Neuropsychol. 2003;25(5):625–633. https://doi.org/10.1076/jcen.25.5.625.14576
41. Stern Y. Cognitive reserve in ageing and Alzheimer’s disease. Lancet Neurol. 2012;11(11):1006–1012. https://doi.org/10.1016/S1474-4422(12)70191-6
42. Schwartz C.E., Snook E., Quaranto B., Benedict R.H.B., Vollmer T. Cognitive Reserve and Patient-Reported Outcomes in Multiple Sclerosis. Mult. Scler. Houndmills Basingstoke Engl. 2013;19(1):87–105. https://doi.org/10.1177/1352458512444914
43. Schwartz C.E., Quaranto B.R., Healy B.C., Benedict R.H., Vollmer T.L. Cognitive Reserve and Symptom Experience in Multiple Sclerosis: A Buff er to Disability Progression over Time?Arch. Phys. Med. Rehabil. 2013;94(10):1971–1981. https://doi.org/10.1016/j.apmr.2013.05.009
44. Chiaravalloti N.D., Moore N.B., Nikelshpur O.M., DeLuca J. An RCT to Treat Learning Impairment in Multiple Sclerosis: The MEMREHAB Trial. Neurology. 2013;81(24):2066–2072. https://doi.org/10.1212/01.wnl.0000437295.97946.a8
Neurology. 2013;81(24):2066–2072. https://doi.org/10.1212/01.wnl.0000437295.97946.a8
45. Mattioli F., Stampatori C., Scarpazza C., Parrinello G., Capra R. Persistence of the Eff ects of Attention and Executive Functions Intensive Rehabilitation in Relapsing Remitting Multiple Sclerosis. Mult. Scler. Relat. Disord. 2012;1(4):168–173. https://doi.org/10.1016/j.msard.2012.06.004
46. Charvet L.E., Yang J., Shaw M.T., Sherman K., Haider L., Xu J., Krupp L. B. Cognitive Function in Multiple Sclerosis Improves with Telerehabilitation: Results from a Randomized Controlled Trial. PLoS ONE. 2017;12(5). https://doi.org/10.1371/journal.pone.0177177
47. Motl R.W., Sandroff B.M., DeLuca J. Exercise Training and Cognitive Rehabilitation: A Symbiotic Approach for Rehabilitating Walking and Cognitive Functions in Multiple Sclerosis? Neurorehabil. Neural Repair. 2016;30(6):499–511. https://doi.org/10.1177/1545968315606993
48. McDonnell M.N., Smith A.E., Mackintosh S.F. Aerobic exercise to improve cognitive function in adults with neurological disorders: a systematic review. Arch. Phys. Med. Rehabil. 2011;92(7):1044–1052. https://doi.org/10.1016/j.apmr.2011.01.021
Arch. Phys. Med. Rehabil. 2011;92(7):1044–1052. https://doi.org/10.1016/j.apmr.2011.01.021
49. Benedict R.H.B., Holtzer R., Motl R.W., Foley F.W., Kaur S., Hojnacki D., Weinstock-Guttman B. Upper and Lower Extremity Motor Function and Cognitive Impairment in Multiple Sclerosis. J. Int. Neuropsychol. Soc. 2011;17(4):643–653. https://doi.org/10.1017/S1355617711000403
50. Briken S., Gold S. M., Patra S., Vettorazzi E., Harbs D., Tallner A. et al. Effects of Exercise on Fitness and Cognition in Progressive MS: A Randomized, Controlled Pilot Trial. Mult. Scler. Houndmills Basingstoke Engl. 2014;20(3):382–390. https://doi.org/10.1177/1352458513507358
51. Leavitt V.M., Cirnigliaro C., Cohen A., Farag A., Brooks M., Wecht J.M. et al. Aerobic Exercise Increases Hippocampal Volume and Improves Memory in Multiple Sclerosis: Preliminary Findings. Neurocase. 2014;20(6):695–697. https://doi.org/10.1080/13554794.2013.841951
52. Токарева А.В., Миронова О.В., Москаленко И.С., Болотин А. Э., Ярчиковская Л.В. Формирование навыков ор- ганизации самостоятельных аэробных тренировок у студентов вузов для успешной сдачи экзаменационной сессии. Теория и практика физической культуры. 2016;9. [Tokareva A.V., Mironova O.V., Moskalenko I.S., Bolotin A.E., Yarchikovskaya L.V. Formation of skills for organizing independent aerobic training for University students to successfully pass the examination session. Theory and practice of physical culture. 2016;9. (In Russian)]. URL: https://cyberleninka.ru/article/n/formirovanie-navykov-organizatsii-samostoyatelnyh-aerobnyhtrenirovok-u-studentov-vuzov-dlya-uspeshnoy-sdachi-ekzamenatsionnoy-sessii/viewer
Э., Ярчиковская Л.В. Формирование навыков ор- ганизации самостоятельных аэробных тренировок у студентов вузов для успешной сдачи экзаменационной сессии. Теория и практика физической культуры. 2016;9. [Tokareva A.V., Mironova O.V., Moskalenko I.S., Bolotin A.E., Yarchikovskaya L.V. Formation of skills for organizing independent aerobic training for University students to successfully pass the examination session. Theory and practice of physical culture. 2016;9. (In Russian)]. URL: https://cyberleninka.ru/article/n/formirovanie-navykov-organizatsii-samostoyatelnyh-aerobnyhtrenirovok-u-studentov-vuzov-dlya-uspeshnoy-sdachi-ekzamenatsionnoy-sessii/viewer
53. Nokia M.S., Lensu S., Ahtiainen J.P., Johansson P.P., Koch L.G., Britton S.L., Kainulainen H. Physical Exercise Increases Adult Hippocampal Neurogenesis in Male Rats Provided It Is Aerobic and Sustained. J. Physiol. 2016;594(7):1855–1873. https://doi.org/10.1113/JP271552
54. Cooper C., Moon H.Y., van Praag H. On the Run for Hippocampal Plasticity. Cold Spring Harb. Perspect. Med. 2018;8:4. https://doi.org/10.1101/cshperspect.a029736
Cold Spring Harb. Perspect. Med. 2018;8:4. https://doi.org/10.1101/cshperspect.a029736
55. Smith-Ray R.L., Hughes S.L., Prohaska T.R., Little D.M., Jurivich D.A., Hedeker D. Impact of Cognitive Training on Balance and Gait in Older Adults. J. Gerontol. B. Psychol. Sci. Soc. Sci. 2015;70(3):357–366. https://doi.org/10.1093/geronb/gbt097
56. Smith-Ray R.L., Makowski-Woidan B., Hughes S.L. A Randomized Trial to Measure the Impact of a Community-Based Cognitive Training Intervention on Balance and Gait in Cognitively Intact Black Older Adults. Health Educ. Behav. Off. Publ. Soc. Public Health Educ. 2014;41(1Suppl):62S–9S. https://doi.org/10.1177/1090198114537068
57. Ball K., Berch D.B., Helmers K.F., Jobe J.B., Leveck M.D., Marsiske M. et al. Advanced Cognitive Training for Independent and Vital Elderly Study Group. Eff ects of Cognitive Training Interventions with Older Adults: A Randomized Controlled Trial. JAMA 2002;288(18):2271–2281. https://doi.org/10.1001/jama.288.18. 2271
2271
Когнитивный резерв при старении и болезни Альцгеймера
1. Гурланд Б. Границы деменции: влияние социокультурных характеристик на частоту деменции, возникающей в старческом возрасте. Старение. 1981; 15: 61–84. [Google Scholar]
2. Kittner SJ, White LR, Farmer ME, Wolz M, Kaplan E, Moes E, et al. Методологические вопросы скрининга деменции: проблема адаптации образования. Журнал хронических болезней. 1986; 39: 163–170. [PubMed] [Google Scholar]
3. Беркман Л.Ф. Связь между уровнем образования и обследованиями психического статуса: имеет этиологическое значение для старческого слабоумия или нет? Журнал хронических болезней. 1986;39:171–174. [PubMed] [Google Scholar]
4. Zhang M, Katzman R, Salmon D, Jin H, Cai G, Wang Z, et al. Распространенность деменции и болезни Альцгеймера в Шанхае, Китай: влияние возраста, пола и образования. Анналы неврологии. 1990; 27: 428–437. [PubMed] [Google Scholar]
5. Elkins JS, Longstreth WT, Manolio TA, Newman AB, Bhadelia RA, Johnston SC. Образование и снижение когнитивных функций, связанные с инфарктом головного мозга, определенным с помощью МРТ. Неврология. 2006;67(3):435–440. [PubMed] [Академия Google]
Образование и снижение когнитивных функций, связанные с инфарктом головного мозга, определенным с помощью МРТ. Неврология. 2006;67(3):435–440. [PubMed] [Академия Google]
6. Dufouil C, Alperovitch A, Tzourio C. Влияние образования на взаимосвязь между поражениями белого вещества и познанием. Неврология. 2003;60(5):831–836. [PubMed] [Google Scholar]
7. Dufouil C, Alperovitch A, Ducros V, Tzourio C. Гомоцистеин, гиперинтенсивность белого вещества и когнитивные функции у здоровых пожилых людей. Энн Нейрол. 2003;53(2):214–221. [PubMed] [Google Scholar]
8. Glatt SL, Hubble JP, Lyons K, Paolo A, Troster AI, Hassanein RE, et al. Факторы риска деменции при болезни Паркинсона: влияние образования. Нейроэпидемиология. 1996;15:20–25. [PubMed] [Google Scholar]
9. Kesler SR, Adams HF, Blasey CM, Bigler ED, et al. Преморбидное интеллектуальное функционирование, образование и размер мозга при черепно-мозговой травме: исследование гипотезы когнитивного резерва. Прикладная нейропсихология. 2003; 10: 153–162. [PubMed] [Google Scholar]
2003; 10: 153–162. [PubMed] [Google Scholar]
10. Farinpour R, Miller EN, Satz P, Selnes OA, Cohen BA, Becker JT, et al. Психосоциальные факторы риска заболеваемости и смертности от ВИЧ: результаты многоцентрового когортного исследования СПИДа (MACS), журнал клинической и экспериментальной нейропсихологии. 2003; 25: 654–670. [PubMed] [Академия Google]
11. Барнетт Дж.Х., Салмонд К.Х., Джонс П.Б., Саакян Б.Дж. Когнитивный резерв в нейропсихиатрии. Психологическая медицина. 2006; 36: 1053–1064. [PubMed] [Google Scholar]
12. Sumowski JF, Chiaravalloti N, Deluca J. Когнитивный резерв защищает от когнитивной дисфункции при рассеянном склерозе. J Clin Exp Neuropsychol. 2009;31(8):913–926. [PubMed] [Google Scholar]
13. Katzman R, Robert T, DeTeresa R, Brown T, Peter D, Fuld P, et al. Клинико-патологические и нейрохимические изменения при деменции: подгруппа с сохраненным психическим статусом и многочисленными неокортикальными бляшками. Анналы неврологии. 1988;23(2):138–144. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
14. Шофилд П.В., Логроскино Г., Эндрюс Х., Альберт С., Стерн Ю. Связь между окружностью головы и болезнью Альцгеймера в популяционном исследовании старения. Неврология. 1997; 49:30–37. [PubMed] [Google Scholar]
15. Стерн Ю. Что такое когнитивный резерв? Теория и исследовательское применение резервной концепции. Журнал Международного нейропсихологического общества. 2002; 8: 448–460. [PubMed] [Google Scholar]
16. Стерн Ю. Когнитивный резерв. Нейропсихология. 2009 г.;47:2015–2028. [Бесплатная статья PMC] [PubMed] [Google Scholar]
17. Браун Дж., Купер-Кун С.М., Кемперман Г., ван Прааг Х., Винклер Дж., Гейдж Ф.Х. Обогащенная окружающая среда и физическая активность стимулируют нейрогенез гиппокампа, но не обонятельной луковицы. ЕВРОПЕЙСКИЙ ЖУРНАЛ НЕВРОНАУКИ. 2003;17:2042–2046. [PubMed] [Google Scholar]
18. van Praag H, Christie BR, Sejnowski TJ, Gage FH. Бег усиливает нейрогенез, обучение и долговременную потенциацию у мышей. Proc Natl Acad Sci U S A. 1999;96(23):13427–13431. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Proc Natl Acad Sci U S A. 1999;96(23):13427–13431. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. van Praag H, Kemperman G, Gage FH. Бег увеличивает пролиферацию клеток и нейрогенез в зубчатой извилине взрослых мышей. Неврология природы. 1999; 2: 266–270. [PubMed] [Google Scholar]
20. van Praag H, Kempermann G, Gage FH. Нейронные последствия обогащения окружающей среды. Нат Рев Нейроски. 2000;1(3):191–198. [PubMed] [Google Scholar]
21. Valenzuela MJ, Sachdev P, Wen W, Chen X, Brodaty H. Умственная активность в течение жизни предсказывает снижение скорости атрофии гиппокампа. ПЛОС Один. 2008;3(7):e2598. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Landau SM, Marks SM, Mormino EC, Rabinovici GD, Oh H, O’Neil JP, et al. Ассоциация когнитивной активности на протяжении всей жизни и низкого уровня бета-амилоидных отложений. Арх Нейрол. 2012 [бесплатная статья PMC] [PubMed] [Google Scholar]
23. Stern Y, Gurland B, Tatemichi TK, Tang MX, Wilder D, Mayeux R. Влияние образования и профессии на заболеваемость болезнью Альцгеймера. Журнал Американской медицинской ассоциации. 1994; 271:1004–1010. [PubMed] [Академия Google]
Влияние образования и профессии на заболеваемость болезнью Альцгеймера. Журнал Американской медицинской ассоциации. 1994; 271:1004–1010. [PubMed] [Академия Google]
24. Scarmeas N, Levy G, Tang MX, Manly J, Stern Y. Влияние досуга на заболеваемость болезнью Альцгеймера. Неврология. 2001;57(12):2236–2242. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Валенсуэла М.Дж., Сачдев П. Мозговой резерв и деменция: систематический обзор. Психомед. 2005; 25:1–14. [PubMed] [Google Scholar]
26. Stern Y, Tang MX, Denaro J, Mayeux R. Повышенный риск смертности у пациентов с болезнью Альцгеймера с более высоким уровнем образования и профессиональной подготовки. Анналы неврологии. 1995;37:590–595. [PubMed] [Google Scholar]
27. Stern Y, Albert S, Tang MX, Tsai WY. Скорость снижения памяти при БА связана с образованием и родом занятий: Когнитивный резерв? Неврология. 1999; 53: 1942–1957. [PubMed] [Google Scholar]
28. Скармиас Н., Альберт С.М., Мэнли Дж.Дж. , Стерн Ю. Образование и темпы снижения когнитивных функций при болезни Альцгеймера. Журнал неврологии, нейрохирургии и психиатрии. 2006;77(3):308–316. [Бесплатная статья PMC] [PubMed] [Google Scholar]
, Стерн Ю. Образование и темпы снижения когнитивных функций при болезни Альцгеймера. Журнал неврологии, нейрохирургии и психиатрии. 2006;77(3):308–316. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Helzner EP, Scarmeas N, Cosentino S, Portet F, Stern Y. Активность в свободное время и снижение когнитивных функций при заболевании болезнью Альцгеймера. Архив неврологии. 2007;64(12):1749–1754. [PubMed] [Google Scholar]
30. Friedland RP, Brun A, Bundinger TF. Патологические и позитронно-эмиссионные томографические корреляции при болезни Альцгеймера. Ланцет. 1985: 1–228. [PubMed] [Google Scholar]
31. McGeer EG, Peppard RP, McGeer PL, et al. 18 Исследования позитронно-эмиссионной томографии с фтордезоксиглюкозой при подозрении на болезнь Альцгеймера, включая 13 последовательных сканирований. Канадский журнал неврологических наук. 1990;17:1–11. [PubMed] [Google Scholar]
32. Stern Y, Alexander GE, Prohovnik I, Mayeux R. Обратная связь между образованием и теменно-височным дефицитом перфузии при болезни Альцгеймера. Анналы неврологии. 1992; 32: 371–375. [PubMed] [Google Scholar]
Анналы неврологии. 1992; 32: 371–375. [PubMed] [Google Scholar]
33. Stern Y, Alexander GE, Prohovnik I, Stricks L, Link B, Lennon MC, et al. Взаимосвязь между занятием на протяжении всей жизни и пристеночным кровотоком: последствия для резерва против патологии болезни Альцгеймера. Неврология. 1995; 45: 55–60. [PubMed] [Академия Google]
34. Scarmeas N, Zarahn E, Anderson KE, Habeck CG, Hilton J, Flynn J, et al. Связь жизнедеятельности с мозговым кровотоком при болезни Альцгеймера — значение для гипотезы когнитивного резерва. Архив неврологии. 2003; 60: 359–365. [Бесплатная статья PMC] [PubMed] [Google Scholar]
35. Alexander GE, Furey ML, Grady CL, Pietrini P, Brady DR, Mentis MJ, et al. Связь преморбидной интеллектуальной функции с церебральным метаболизмом при болезни Альцгеймера: значение для гипотезы когнитивного резерва. Am J Психиатрия. 1997;154(2):165–172. [PubMed] [Google Scholar]
36. Perneczky R, Drzezga A, ehl-Schmid J, Schmid G, Wohlschlager A, Kars S, et al. Обучение в школе опосредует резерв мозга при болезни Альцгеймера: результаты фтор-дезокси-глюкозо-позитронно-эмиссионной томографии. J Neurol Нейрохирург Психиатрия. 2006;77(9):1060–1063. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Обучение в школе опосредует резерв мозга при болезни Альцгеймера: результаты фтор-дезокси-глюкозо-позитронно-эмиссионной томографии. J Neurol Нейрохирург Психиатрия. 2006;77(9):1060–1063. [Бесплатная статья PMC] [PubMed] [Google Scholar]
37. Bennett DA, Wilson RS, Schneider JA, Evans DA, Mendes De Leon CF, Arnold SE, et al. Образование модифицирует отношение патологии БА к уровню когнитивной функции у пожилых людей. Неврология. 2003;60(12):1909–1915. [PubMed] [Google Scholar]
38. Stern Y, Habeck C, Moeller J, Scarmeas N, Anderson KE, Hilton HJ, et al. Сети мозга, связанные с когнитивным резервом у здоровых молодых и пожилых людей. Кора головного мозга. 2005;15(4):394–402. [Бесплатная статья PMC] [PubMed] [Google Scholar]
39. Stern Y, Rakitin BC, Habeck C, Gazes Y, Steffener J, Kumar A, et al. Сложность задачи модулирует различия между молодыми и старыми в выражении сети. Мозг Res. 2012;1435:130–145. [Бесплатная статья PMC] [PubMed] [Google Scholar]
40. Заран Э., Ракитин Б., Абела Д., Флинн Дж., Стерн Ю. Возрастные изменения в активации мозга во время задачи распознавания предметов с задержкой. Нейробиол Старение. 2007;28(5):784–798. [PubMed] [Google Scholar]
Заран Э., Ракитин Б., Абела Д., Флинн Дж., Стерн Ю. Возрастные изменения в активации мозга во время задачи распознавания предметов с задержкой. Нейробиол Старение. 2007;28(5):784–798. [PubMed] [Google Scholar]
41. Steffener J, Brickman AM, Rakitin BC, Gazes Y, Stern Y. Влияние структуры на возрастные изменения функциональной активности рабочей памяти. Визуализация мозга и поведение. 2008 [Бесплатная статья PMC] [PubMed] [Google Scholar]
42. Стеффенер Дж., Рубен А., Ракитин Б.С., Стерн Ю. Поддержка производительности перед лицом возрастных нейронных изменений: проверка механистической роли когнитивного резерва. Поведение визуализации мозга. 2011 [Бесплатная статья PMC] [PubMed] [Google Scholar]
43. Стерн Ю., Заран Э., Хабек С., Хольцер Р., Ракитин Б.С., Кумар А. и соавт. Общая нейронная сеть для когнитивного резерва в вербальной и объектной рабочей памяти у молодых, но не старых. Кора головного мозга. 2008; 18: 959–967. [Бесплатная статья PMC] [PubMed] [Google Scholar]
44. Garibotto V, Borroni B, Kalbe E, Herholz K, Salmon E, Holtoff V, et al. Образование и профессия как показатели резерва в преобразователях aMCI и AD: свидетельство FDG-PET. Неврология. 2008;71(17):1342–1349. [PubMed] [Академия Google]
Garibotto V, Borroni B, Kalbe E, Herholz K, Salmon E, Holtoff V, et al. Образование и профессия как показатели резерва в преобразователях aMCI и AD: свидетельство FDG-PET. Неврология. 2008;71(17):1342–1349. [PubMed] [Академия Google]
45. Кемппайнен Н.М., Аалто С., Карраш М., Нагрен К., Сависто Н., Ойконен В. и соавт. Гипотеза когнитивного резерва: Питтсбургское соединение B и позитронно-эмиссионная томография с фтордезоксиглюкозой в отношении образования при легкой болезни Альцгеймера. Энн Нейрол. 2008;63(1):112–118. [PubMed] [Google Scholar]
46. Hall CB, Derby C, LeValley A, Katz MJ, Verghese J, Lipton RB. Образование задерживает ускоренное ухудшение результатов теста памяти у лиц, у которых развивается слабоумие. Неврология. 2007;69(17):1657–1664. [PubMed] [Академия Google]
47. Angevaren M, Aufdemkampe G, Verhaar H, Aleman A, Vanhees L. Физическая активность и улучшение физической формы для улучшения когнитивных функций у пожилых людей без известных когнитивных нарушений. Кокрановская система базы данных, ред. 2008; 2 CD005381. [PubMed] [Google Scholar]
Кокрановская система базы данных, ред. 2008; 2 CD005381. [PubMed] [Google Scholar]
48. Kramer AF, Hahn S, Cohen NJ, Banich MT, McAuley E, Harrison CR, et al. Старение, фитнес и нейрокогнитивные функции. Природа. 1999;400(6743):418–419. [PubMed] [Google Scholar]
49. Jobe JB, Smith DM, Ball K, Tennstedt SL, Marsiske M, Willis SL, et al. АКТИВНЫЙ: испытание когнитивной интервенции для развития самостоятельности у пожилых людей. Контрольные клинические испытания. 2001; 22(4):453–479.. [Бесплатная статья PMC] [PubMed] [Google Scholar]
50. Basak C, Boot WR, Voss MW, Kramer AF. Могут ли тренировки в стратегической видеоигре в реальном времени смягчить снижение когнитивных функций у пожилых людей? Психология и старение. 2008;23(4):765–777. [PMC free article] [PubMed] [Google Scholar]
51. Клингберг Т. Тренировка и пластичность рабочей памяти. Тенденции Cogn Sci. 2010;14(7):317–324. [PubMed] [Google Scholar]
52. Wykes T, Huddy V, Cellard C, McGurk SR, Czobor P. Метаанализ когнитивной реабилитации при шизофрении: методология и размеры эффекта. Am J Психиатрия. 2011;168(5):472–485. [PubMed] [Академия Google]
Метаанализ когнитивной реабилитации при шизофрении: методология и размеры эффекта. Am J Психиатрия. 2011;168(5):472–485. [PubMed] [Академия Google]
53. Королевское общество. Мозговые волны Модуль 2: Неврология: последствия для образования и обучения на протяжении всей жизни. 2011 [цит.; Доступно по адресу: http://royalsociety.org/uploadedFiles/Royal_Society/Policy_and_Influence/Module_2_Neuroscience_Education_Full_Report_Printer_Friendly.pdf.
54. Мане АДЭ. Игра «Космическая крепость». Acta Psychologica. 1989; 71: 17–22. [Google Scholar]
55. Fabiani M, Buckley J, Gratton G, Coles MGH, Donchin E. Обучение выполнению сложных задач. Acta Psychologica. 1989;71:259–299. [Google Scholar]
56. Гофер Д., Вейл М., Барекет Т. Перенос навыков из тренажера компьютерных игр в полет. Человеческие факторы. 1994;36(3):387–405. [Google Scholar]
57. Гофер Д., Вейл М., Сигал Д. Практика в условиях меняющихся приоритетов: подход к обучению сложным навыкам. Acta Psychologica. 1989; 71: 147–177. [Google Scholar]
1989; 71: 147–177. [Google Scholar]
58. Blumen HM, Gopher D, Steinerman JR, Stern Y. Тренировка когнитивного контроля у пожилых людей с помощью игры «Космическая крепость»: роль тренировочных инструкций и базовых двигательных способностей. Front Aging Neurosci. 2010;2:145. [Бесплатная статья PMC] [PubMed] [Google Scholar]
59. Оррелл М., Саакян Б. Образование и деменция. БМЖ. 1995;310(6985):951–952. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Когнитивный резерв при старении и болезни Альцгеймера
Обзор
. 2012 ноябрь;11(11):1006-12.
doi: 10.1016/S1474-4422(12)70191-6.
Яаков Штерн 1
принадлежность
- 1 Отделение когнитивной неврологии, отделение неврологии и Институт Тауба, Колледж врачей и хирургов Колумбийского университета, Нью-Йорк, NY 10032, США.
 [email protected]
[email protected]
- PMID: 23079557
- PMCID: PMC3507991
- DOI: 10.1016/С1474-4422(12)70191-6
Бесплатная статья ЧВК
Обзор
Яаков Штерн. Ланцет Нейрол. 2012 ноябрь
Бесплатная статья ЧВК
. 2012 ноябрь;11(11):1006-12.
дои: 10.1016/S1474-4422(12)70191-6.
Автор
Яаков Штерн 1
принадлежность
- 1 Отделение когнитивной неврологии, отделение неврологии и Институт Тауба, Колледж врачей и хирургов Колумбийского университета, Нью-Йорк, NY 10032, США.
 [email protected]
[email protected]
- PMID: 23079557
- PMCID: PMC3507991
- DOI: 10.1016/С1474-4422(12)70191-6
Абстрактный
Концепция когнитивного резерва объясняет различия между людьми в восприимчивости к возрастным изменениям мозга или патологии, связанной с болезнью Альцгеймера, при этом некоторые люди могут переносить больше этих изменений, чем другие, и сохранять функцию. Эпидемиологические исследования показывают, что жизненный опыт, включая образовательные и профессиональные достижения, а также досуг в более позднем возрасте, может увеличить этот резерв. Например, риск развития болезни Альцгеймера снижается у лиц с высшим образованием или профессиональным образованием. Резерв можно условно разделить на два типа: резерв мозга, который относится к различиям в структуре мозга, которые могут повышать устойчивость к патологии, и когнитивный резерв, который относится к различиям между людьми в том, как выполняются задачи, которые могут позволить некоторым людям быть более продуктивными. устойчивы к мозговым изменениям, чем другие. Лучшее понимание концепции когнитивного резерва может привести к вмешательствам, замедляющим когнитивное старение или снижающим риск деменции.
Резерв можно условно разделить на два типа: резерв мозга, который относится к различиям в структуре мозга, которые могут повышать устойчивость к патологии, и когнитивный резерв, который относится к различиям между людьми в том, как выполняются задачи, которые могут позволить некоторым людям быть более продуктивными. устойчивы к мозговым изменениям, чем другие. Лучшее понимание концепции когнитивного резерва может привести к вмешательствам, замедляющим когнитивное старение или снижающим риск деменции.
Copyright © 2012 Elsevier Ltd. Все права защищены.
Заявление о конфликте интересов
Конфликта интересов нет.
Цифры
Рисунок 1
Эта гипотетическая цифра иллюстрирует, как…
Рисунок 1
Этот гипотетический рисунок иллюстрирует, как со временем изменяется функция памяти у людей с…
Рисунок 1 Этот гипотетический рисунок иллюстрирует, как со временем изменяется функция памяти у людей с высоким и низким резервом. При отсутствии патологии БА вполне вероятно, что люди с более высоким резервом будут лучше выполнять тесты на память, хотя это не всегда наблюдалось. Патология AD начинает прогрессировать до любого наблюдения за изменением производительности памяти. Однако в какой-то момент патологии достаточно, чтобы начать вызывать заметное снижение показателей тестов памяти. Этот момент, когда производительность начинает снижаться, наступает позже у людей с более высоким резервом, потому что они могут переносить больше патологии, прежде чем она повлияет на производительность. На рисунке показана точка, в которой патология настолько серьезна, что производительность памяти равна нулю. Этот момент одинаков как для людей с высоким, так и с низким резервом. Учитывая эту общую конечную точку, рисунок предполагает, что, как только ухудшение памяти действительно начнется, скорость снижения должна быть более высокой у людей с более высоким резервом, чем у людей с более низким резервом. Эта теоретическая модель может объяснить наблюдения более быстрого клинического снижения у пациентов с БА с более высоким резервом.
При отсутствии патологии БА вполне вероятно, что люди с более высоким резервом будут лучше выполнять тесты на память, хотя это не всегда наблюдалось. Патология AD начинает прогрессировать до любого наблюдения за изменением производительности памяти. Однако в какой-то момент патологии достаточно, чтобы начать вызывать заметное снижение показателей тестов памяти. Этот момент, когда производительность начинает снижаться, наступает позже у людей с более высоким резервом, потому что они могут переносить больше патологии, прежде чем она повлияет на производительность. На рисунке показана точка, в которой патология настолько серьезна, что производительность памяти равна нулю. Этот момент одинаков как для людей с высоким, так и с низким резервом. Учитывая эту общую конечную точку, рисунок предполагает, что, как только ухудшение памяти действительно начнется, скорость снижения должна быть более высокой у людей с более высоким резервом, чем у людей с более низким резервом. Эта теоретическая модель может объяснить наблюдения более быстрого клинического снижения у пациентов с БА с более высоким резервом. Согласно этой модели, эта дифференциальная скорость снижения может наблюдаться как у лиц, у которых уже диагностирована болезнь Альцгеймера, так и у тех, у кого память начала ухудшаться.
Согласно этой модели, эта дифференциальная скорость снижения может наблюдаться как у лиц, у которых уже диагностирована болезнь Альцгеймера, так и у тех, у кого память начала ухудшаться.
Рисунок 2
Клинические проявления когнитивного резерва…
Рисунок 2
Клинические проявления когнитивного резерва. Этот рисунок описывает теоретические эффекты различных…
фигура 2 Клинические проявления когнитивного резерва. На этом рисунке показаны теоретические эффекты различных уровней патологии болезни Альцгеймера по оси x и клинической тяжести по оси y. Когда патология AD легкая, люди с более низким уровнем резерва могут уже казаться клинически слабоумными, в то время как люди с более высоким резервом могут казаться клинически нормальными. При более высоких уровнях патологии обе группы могут оказаться клинически слабоумными. Тем не менее, люди с более высоким резервом будут менее клинически выражены, чем люди с более низким резервом.
При более высоких уровнях патологии обе группы могут оказаться клинически слабоумными. Тем не менее, люди с более высоким резервом будут менее клинически выражены, чем люди с более низким резервом.
Рисунок 3
Это цифра из…
Рисунок 3
Это цифра из нашего первого исследования, которое проверило идею о том, что…
Рисунок 3 Это цифра из нашего первого исследования, в котором проверялась идея о том, что при любом заданном уровне клинической тяжести пациенты с БА с более высоким CR должны иметь более выраженную патологию БА. В этом исследовании мы использовали показатель мозгового кровотока в качестве показателя патологии AD. На рисунке представлены три группы из 20 пациентов с БА, все тщательно подобранные по клинической тяжести, измеряемой психическим статусом и активностью в повседневной жизни. Обратите внимание, что группа с самым высоким уровнем образования имеет самый темный синий цвет в теменно-височной области, что указывает на самый низкий уровень кровотока и, в свою очередь, на наиболее продвинутую патологию БА. Эта цифра предполагает, что, несмотря на то, что три группы сопоставимы по клинической тяжести, у лиц с более высоким уровнем образования более высокий уровень лежащей в основе патологии.
Обратите внимание, что группа с самым высоким уровнем образования имеет самый темный синий цвет в теменно-височной области, что указывает на самый низкий уровень кровотока и, в свою очередь, на наиболее продвинутую патологию БА. Эта цифра предполагает, что, несмотря на то, что три группы сопоставимы по клинической тяжести, у лиц с более высоким уровнем образования более высокий уровень лежащей в основе патологии.
См. это изображение и информацию об авторских правах в PMC
Похожие статьи
Когнитивный резерв в старости.
Такер А.М., Стерн Ю. Такер А.М. и др. Curr Alzheimer Res. 2011 июнь;8(4):354-60. дои: 10.2174/156720511795745320. Curr Alzheimer Res. 2011. PMID: 21222591 Бесплатная статья ЧВК. Обзор.
Баланс между когнитивным резервом и биомаркерами визуализации головного мозга при цереброваскулярных заболеваниях и болезни Альцгеймера.

Мюррей А.Д., Штат Р.Т., Макнил С.Дж., Саларирад С., Ахерн Т.С., Мустафа Н., Уолли Л.Дж. Мюррей А.Д. и соавт. Мозг. 2011 декабрь; 134 (часть 12): 3687-96. doi: 10.1093/мозг/awr259. Epub 2011 18 ноября. Мозг. 2011. PMID: 22102649
[Опросник когнитивного резерва. Баллы, полученные у здорового пожилого населения и у одного с болезнью Альцгеймера].
Рами Л., Вальс-Педре С., Бартрес-Фаз Д., Каприль С., Соле-Падульес С., Кастельви М., Оливес Дж., Бош Б., Молинуево Дж.Л. Рами Л. и др. Преподобный Нейрол. 2011 16 февраля; 52 (4): 195-201. Преподобный Нейрол. 2011. PMID: 21312165 Испанский язык.
Когнитивный резерв и его значение для реабилитации и болезни Альцгеймера.
Либерати Г.
 , Раффоне А., Оливетти Белардинелли М.
Либерати Г. и др.
Процесс познания. 2012 Февраль;13(1):1-12. дои: 10.1007/s10339-011-0410-3. Epub 2011 4 июня.
Процесс познания. 2012.
PMID: 21643921
Обзор.
, Раффоне А., Оливетти Белардинелли М.
Либерати Г. и др.
Процесс познания. 2012 Февраль;13(1):1-12. дои: 10.1007/s10339-011-0410-3. Epub 2011 4 июня.
Процесс познания. 2012.
PMID: 21643921
Обзор.Когнитивный резерв: последствия для оценки и вмешательства.
Стерн Ю. Стерн Ю. Фолиа Фониатр Логотип. 2013;65(2):49-54. дои: 10.1159/000353443. Epub 2013 12 августа. Фолиа Фониатр Логотип. 2013. PMID: 23941972 Бесплатная статья ЧВК.
Посмотреть все похожие статьи
Цитируется
Устойчивость нейронной клеточности к влиянию низкого образовательного уровня.
де Мораис В.А.К., де Оливейра-Пинто А.В., Мелло Нето А.Ф., Фрейташ Х.С., да Силва М.
 М., Суемото К.К., Лейте Р.П., Гринберг Л.Т., Джейкоб-Фильо В., Паскуалуччи К., Нитрини Р., Карамелли П., Лент Р.
де Морайс ВАК и др.
наук о мозге. 2023 5 января; 13 (1): 104. doi: 10.3390/brainsci13010104.
наук о мозге. 2023.
PMID: 36672086
Бесплатная статья ЧВК.
М., Суемото К.К., Лейте Р.П., Гринберг Л.Т., Джейкоб-Фильо В., Паскуалуччи К., Нитрини Р., Карамелли П., Лент Р.
де Морайс ВАК и др.
наук о мозге. 2023 5 января; 13 (1): 104. doi: 10.3390/brainsci13010104.
наук о мозге. 2023.
PMID: 36672086
Бесплатная статья ЧВК.Влияние повреждения сети белого вещества и преморбидных интеллектуальных способностей на послеоперационную вербальную кратковременную память и функциональный результат у пациентов с поражениями головного мозга.
Эбина К., Мацуи М., Киношита М., Сайто Д., Накада М. Эбина К. и соавт. ПЛОС Один. 2023 20 января; 18 (1): e0280580. doi: 10.1371/journal.pone.0280580. Электронная коллекция 2023. ПЛОС Один. 2023. PMID: 36662758 Бесплатная статья ЧВК.
Многокомпонентные вмешательства у пожилых людей с субъективным снижением когнитивных функций (SCD) — обзорная статья.

Моханти М., Кумар П. Моханти М. и др. Гериатрия (Базель). 2022 27 декабря; 8 (1): 4. doi: 10.3390/geriatrics8010004. Гериатрия (Базель). 2022. PMID: 36648909 Бесплатная статья ЧВК. Обзор.
Вмешательство до и после вмешательства исследует когнитивные функции и взаимосвязь с потерей веса, приверженностью к вмешательству и отсевом.
Сабо-Рид А.Н., Мартин Л.Е., Сэвидж К.Р., Уошберн Р.А., Доннелли Д.Е. Сабо-Рид А.Н. и соавт. Health Psychol Behav Med. 2023 6 января; 11 (1): 2162528. дои: 10.1080/21642850.2022.2162528. Электронная коллекция 2023. Health Psychol Behav Med. 2023. PMID: 36632603 Бесплатная статья ЧВК.
Признание социального здоровья: концептуальная основа в контексте исследования деменции.




 , Раффоне А., Оливетти Белардинелли М.
Либерати Г. и др.
Процесс познания. 2012 Февраль;13(1):1-12. дои: 10.1007/s10339-011-0410-3. Epub 2011 4 июня.
Процесс познания. 2012.
PMID: 21643921
Обзор.
, Раффоне А., Оливетти Белардинелли М.
Либерати Г. и др.
Процесс познания. 2012 Февраль;13(1):1-12. дои: 10.1007/s10339-011-0410-3. Epub 2011 4 июня.
Процесс познания. 2012.
PMID: 21643921
Обзор. М., Суемото К.К., Лейте Р.П., Гринберг Л.Т., Джейкоб-Фильо В., Паскуалуччи К., Нитрини Р., Карамелли П., Лент Р.
де Морайс ВАК и др.
наук о мозге. 2023 5 января; 13 (1): 104. doi: 10.3390/brainsci13010104.
наук о мозге. 2023.
PMID: 36672086
Бесплатная статья ЧВК.
М., Суемото К.К., Лейте Р.П., Гринберг Л.Т., Джейкоб-Фильо В., Паскуалуччи К., Нитрини Р., Карамелли П., Лент Р.
де Морайс ВАК и др.
наук о мозге. 2023 5 января; 13 (1): 104. doi: 10.3390/brainsci13010104.
наук о мозге. 2023.
PMID: 36672086
Бесплатная статья ЧВК.
